Влияние - концентрация - ион - водород
Cтраница 1
Влияние концентрации ионов водорода и хлора на продолжительность реакции диазотирования ( Т0 С Самина 0.001 г-мол. [1]
Влияние концентрации ионов водорода на гидролиз фосфорсодержащих эфиров в настоящее время хорошо изучено и, по-видимому, имеется общая закономерность [129, 130, 140] ( см. также стр. Так, для моноалкилфосфатов, например метилфосфата, скорость гидролиза имеет максимум при рН 4 0, снижается при рН 1 0 и затем возрастает в сильных кислотах. Наличие как ОН, так и О - рядом с фосфором является необходимым для подобного катализа. В частности, диэфиры более стабильны, чем моноэфиры. [2]
Влияние концентрации ионов водорода исследовали неоднократно. [3]
Влияние концентрации ионов водорода тга растворимость было исследовано на примере р - ( а-нафтил) - р-аланина. [4]
Такое влияние концентрации ионов водорода на направление самопроизвольной реакции используется при промышленном получении брома. [5]
Изучено влияние концентраций ионов водорода и высаливателя на экстракцию серебра из азотнокислых растворов сульфидами. На рис. 12 показано, что концентрация ионов водорода не влияет на экстракцию серебра. Введение высаливателя увеличивает коэффициент распределения в соответствии с уравнением ( 2), причем последний не зависит от типа применяемых высаливателей. [6]
При исследовании влияния концентрации ионов водорода в среде, в условиях свободного доступа воздуха, среды с низким рН образовывались раствором различной концентрации соляной кислоты, которая не является окислителем, э поэтому не образует, как, например, серная или азотная кислоты, пассивирующих пленок на поверхности стали. В качестве нейтральных сред в исследованиях были применены вода Львовского водопровода и дистиллированная вода, а щелочные среды с различными рН образовывались растворами различной концентрации едкого натрия. [7]
Для уточнения влияния концентрации ионов водорода в растворе на появление в исследуемых трубах межкристаллитной коррозии был поставлен дополнительный эксперимент. [8]
Таким образом, влияние концентрации ионов водорода на процессы осаждения ионов органическими реактивами имеет довольно сложный характер. В наиболее простых случаях равновесие соответствует приведенному выше уравнению ( 1), и для полного осаждения необходимо уменьшить концентрацию ионов водорода до определенного предела. Однако при дальнейшем уменьшении концентрации ионов водорода иногда, как отмечено выше, возникают новые процессы, в результате которых растворимость осадка повышается. [9]
Важнейшие результаты изучения влияния концентрации ионов водорода на величины перенапряжения состоят в следующем. В наиболее удовлетворительном согласии с теорией А. Н. Фрумкина находятся экспериментальные данные по водородному перенапряжению, полученные для ртутного электрода. [10]
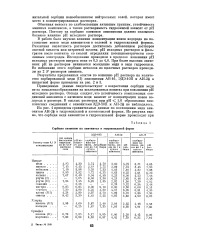 |
Сорбция катионов на анионитах в гидроксильной форме. [11] |
В работе было изучено влияние концентрации ионов водорода на поглощение ионов меди анионитами в солевой и гидроксильной формах. [12]
В результате этого сопоставления обнаружена значительная аналогия во влиянии концентрации ионов водорода на интенсивность электроокисления анилина и на константу поглощения ультрафиолетовых лучей. [13]
Уравнения вида ( 37) и ( 39), отражающие влияние концентрации ионов водорода в промывном растворе на коэффициент распределения, неприменимы к органическим кислотам, за исключением сильно диссоциирующих органических кислот, таких, как щавелевая. Действительно, объем раствора, отвечающий максимальной концентрации иона, при вымывании многих органических кислот, увеличивается при уменьшении рН промывного раствора, а рассматриваемые уравнения предсказывают противоположное. [14]
В случае хлорирования растворов кальцинированной соды по уравнению ( 19) влияние концентрации ионов водорода минимальное, и кривая окислительно-восстановительной системы дает не очень резкий скачок в момент окончания реакции. [15]
Страницы: 1 2