Влияние - атом - сера
Cтраница 2
В предшествующей работе [1] была установлена сравнит льная активность эфиров некоторых фосфористых и фосфиновых кислот как присадок, понижающих износ при трении. Было показано влияние атомов серы и хлора, содержащихся в молекуле этих фосфорорганических соединений, на износ стали при высоких нагрузках. Полученные результаты дали основание предполагать, что наиболее активные синтетические присадки могут быть получены сочетанием в молекуле присадок фосфора и серы и, в особенности, фосфора и хлора. Как показали предварительные исследования, в этом отношении значительный интерес представляют эфиры хлоралкилфосфиновых кислот. [16]
Применение в качестве диазосоставляющих гетероциклических соединений, у которых аминогруппа связана с пятичленным гетероциклом, позволяет получать очень простые моноазокра-сители глубоких цветов. По-видимому, в этом сказывается влияние атома серы ( третий период системы Д. И. Менделеева), имеющего большие размеры 3 / 7-орбиталей по сравнению с 2р - орбиталями атомов углерода и азота, а также вакантные Srf-орбитали, оказывающие влияние на уровень энергии молекул в возбужденном состоянии. [17]
Комплексы Си ( П) с линейными политиоэфирами Etj - rryCIM) и тту ( пожтиоэфир с двумя концевыми SH-группами) также имеют высокие окислительно-восстановительные потенциалы. В этом случае сказывается, по-видимому влия-ние S Н - группы, аналогичное влиянию атома серы тиоэфира. [18]
В нейтральных растворителях ( углеводородах) все ОСС растворяются примерно одинаково. С повышением молекулярной массы растворимость в углеводородах увеличивается, поскольку снижается в молекулярном взаимодействии влияние атома серы. Поскольку склонность к образованию водородной связи ярко выражена у низкомолекулярных ОСС, для них наблюдается наибольшая растворимость в полярных растворителях. Так, в работе [100] показано, что избирательные растворители фенол и фурфурол достаточно полно обессеривают низкокипящие дистилляты. Однако при этом наблюдаются большие потери ценных ароматических углеводородов, экстрагируемых с ОСС. Применена последовательная экстракция, позволяющая улучшить условия обессеривания, уменьшить расход фенола и количество отходов. [19]
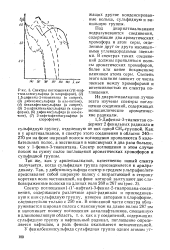 |
Спектры поглощения ( / 1-наф-тилаллилсульфида ( в хлороформе, ( 2 1 5-дифенил - З - тиапентана ( в спирте. [20] |
Под диарилтиаалканами подразумеваются соединения, содержащие два ароматических хромофора и атом серы, отделенные друг от друга насыщен - ными углеводородными звеньями. В спектрах таких соединений должны проявляться полосы ароматических хромофоров, более или менее искаженные влиянием атома серы. Степень этого влияния зависит от числа звеньев между хромофорами и интенсивностью их спектра поглощения. [21]
Алкил-и фенилзамещенные тиофены [174-176] также неактивны в этой реакции. Однако введение заместителей в бензольное кольцо изобензтиофена или конденсация тиофенового кольца с полициклическими ароматическими системами ослабляет влияние атома серы, активирует систему двойных связей тиофенового ядра и делает ее способной к диеновому синтезу. [22]
 |
Спектры поглощения ( / тиант-рена ( в петрвлейном эфире, ( 2 дибен-зилдисульфида ( в изо-октане, ( 5 дифе-нилдисульфида ( в цзо-октане, ( 4 ди-1 - нафтилдисульфида ( в хлороформе. [23] |
Свободные Зр-электроны ( - S-S -) - группы нарушают электронную структуру даже такого активного хромофора, как нафтильный. Спектры поглощения нафталинового хромофора сохранялись в соседстве с сульфогидрильной или сульфидной группой и в них не очень заметно сказывалось влияние атома серы. [24]
Активным промежуточным соединением в переносе ацетата является тиолацетат кофермента А 1103 ], причем этот активный ацетат образуется ферментативно под действием ацетилфосфата [104] или аденилилацетата [105] на кофермент. Тиоловые эфиры, особенно 2-меркаптоэтиламина [106-108] и пантотеина [109-111], представляют собой очень активные химические ацилирующие агенты. Было также обнаружено влияние атома серы, приводящее к освобождению протона из - положения. Ферментативное S-фосфорилирование кофермента А гуано-зин-5 - трифосфатом в дрожжах и сердечной мышце [113] ( но аде-нозин-5 - трифосфатом в других тканях [114]) представляет собой другой путь активации янтарной кислоты. Химическое фосфорили-рование кофермента А хлорокисью фосфора дает, по-видимому, как утверждают [115], тиолфосфат, но более вероятен при этом распад ангидрида или образование 2 3 -циклофосфатного производного. [25]
Страницы: 1 2