Влияние - мицелла
Cтраница 1
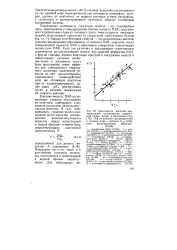 |
Зависимость констант распределения органических соединений между водой и мицеллами ( Рм от констант распределения в системе вода - октанол Яокт, если распределяемое вещество ( ПАВ. [1] |
Влияние мицелл ПАВ на химические реакции обусловлено их свойством сорбировать ( связывать) различные низкомолекулярные вещества. [2]
Следует заметить, что первоначально было изучено влияние мицелл на химическое равновесие. Катализ или ингибирование солюбилизованных веществ включает в себя широкий ряд взаимодействий и может изменяться в зависимости от природы ПАВ. [3]
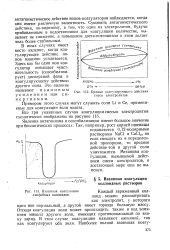 |
Кривые коагулирующего действия смеси электролитов.| Взаимная коагуляция лиофобных коллоидов. [4] |
Отсюда коагуляция золя может происходить также и под влиянием мицелл другого золя, имеющих противоположный по знаку заряд. В этом случае коагуляцию называют взаимной, так как коагулируют оба золя. [5]
Ввиду относительной простоты реакций гидролиза сложных эфиров, в частности щелочного гидролиза, эти процессы служат в качестве модельных в исследованиях влияния мицелл на скорости реакций и активационные параметры. Важность изучения таких реакций определяется также и тем, что они чрезвычайно распространены в биологических системах, где гидролиз сложных эфиров катализируется нуклеофильными агентами или ферментами. [6]
Мицеллы влияют, однако, не только на активность ионов водорода и, таким образом, на р / С, но и на коэффициенты активности индикатора IB и его сопряженной кислоты IA - Последующее изучение влияния мицеллы на функции кислотности Н0 и Ян с использованием в качестве индикаторов Гаммета ( Я0) л-нитро-анилина и 1-амино - 4-нитронафталина и в качестве индикатора на Як N-три-л - анизилметанола показало, что ДДС увеличивает - Ян на 2 5 ед. БЦТА уменьшает Як на 1 4 ед. Значение этих результатов состоит в том, что они показывают невозможность непосредственного определения протонодонорной способности или кислотности в ми-целлярных растворах с помощью индикаторов, поскольку нельзя пренебречь влиянием мицелл на отношение коэффициентов активности двух форм индикатора. [7]
Механизм мицеллярного катализа сложен, зависит от специфики реагентов и ПАВ и выяснен далеко не в полной мере. Влияние мицелл на химические реакции определяется двумя основными факторами - изменением реакционной способности веществ при переходе их из воды в мицелляр-ную фазу и эффектом концентрирования реагентов в мицеллах, причем второй фактор во многих случаях является единственным источником мицеллярного катализа. На роль электростатических взаимодействий указывает, в частности, тот факт, что обычно ре-акции нуклеофильных анионов с нейтральными молекулами ускоряются катионными мицеллами, замедляются анионными, а мицеллы НПАВ практически не оказывают на них влияния. Во многих случаях мицеллы влияют не только на кинетику, но и на равновесие реакций, что не свойственно истинным катализаторам. [8]
Эта работа - первая, в которой наблюдали влияние мицелл на радикальные процессы, индуцированные облучением. [9]
 |
Взаимная коагуляция золей. [10] |
Каждый заряженный коллоид можно рассматривать как электролит, у которого один имеет значительно большую массу, чем другой. Отсюда коагуляция золя может происходить также и под влиянием мицелл другого золя, имеющих противоположный по знаку заряд. В этом случае коагуляцию называют взаимной, так как коагулируют оба золя. Наиболее полной взаимная коагуляция будет тогда, когда число разноименных электрических зарядов на частицах обоих коллоидов будет одинаково. При иных соотношениях коагуляция может не произойти, дисперсная фаза в этом случае будет нести знак того коллоида, который находится в избытке. [11]
Можно думать, что развитая в работе модель расширит возможности кинетических подходов при исследовании структуры мицелл. Константа скорости в мицеллярной фазе km может быть мерой не связанного с концентрационными эффектами влияния мицелл на энергетику реакции. И если величина ионообменной константы К действительно окажется не зависящей от типа изученной реакции, то это будет новый способ измерения относительной способности противо - ионов связываться в мицеллярном слое Штерна. [12]
Нуклеофильное замещение в ароматическом ряду, как правило, протекает по двухступенчатому бимолекулярному механизму, причем лимитирующей стадией может быть образование или распад промежуточного соединения. И в случае алифатических, и в случае ароматических соединений часто образуются заряженные комплексы. Различные изменения зарядов, теоретически возможные в реакциях нуклеофильного замещения, могут быть причиной влияния мицелл на скорость этих реакций. По имеющимся данным, мицеллы влияют на скорости реакций нуклеофильного замещения в алифатическом ряду только в тех случаях, когда хотя бы один из реагентов заряжен. Однако вполне возможно, что будут обнаружены мицеллярные эффекты в реакциях нуклеофильного замещения между нейтральными молекулами в тех случаях, когда распределение реагентов между мицеллами и объемом растворителя, а также их реакционная способность в этих двух фазах сильно различаются. [13]
Мицеллы влияют, однако, не только на активность ионов водорода и, таким образом, на р / С, но и на коэффициенты активности индикатора IB и его сопряженной кислоты IA - Последующее изучение влияния мицеллы на функции кислотности Н0 и Ян с использованием в качестве индикаторов Гаммета ( Я0) л-нитро-анилина и 1-амино - 4-нитронафталина и в качестве индикатора на Як N-три-л - анизилметанола показало, что ДДС увеличивает - Ян на 2 5 ед. БЦТА уменьшает Як на 1 4 ед. Значение этих результатов состоит в том, что они показывают невозможность непосредственного определения протонодонорной способности или кислотности в ми-целлярных растворах с помощью индикаторов, поскольку нельзя пренебречь влиянием мицелл на отношение коэффициентов активности двух форм индикатора. [14]
Поскольку значения K / N для БЦТА, ДДС и неионного ПАВ отличаются незначительно, 2 4-динитрохлорбензол сильно солюбилизуется мицеллами, а малая величина мицеллярного эффекта в реакции гидроксидехлори-рования не является следствием невключения субстрата в мицеллы, а скорее всего объясняется близостью констант скорости в мицел-лярной и водной фазах. Что же касается различий в свободной энергии активации реакции ( 42в) в присутствии и в отсутствие детергентов, то этот эффект - следствие изменений и энтальпии, и энтропии активации. Интерпретация мицеллярно-каталитическо-го эффекта в этом случае не столь проста, как для тех реакций, где катализ связан с изменением только одного вклада в свободную энергию. В водном этиловом спирте влияние мицелл на реакции нуклеофильного замещения качественно аналогично, хотя и менее явно выражено, чем в водных растворах. [15]
Страницы: 1