Влияние - неподеленная пара
Cтраница 1
 |
Валентные углы в молекулах тригидридов и тригалогенидов, град. [1] |
Влияние неподеленной пары всегда приводит к уменьшению валентного угла по сравнению с его значением для правильного тетраэдра. [2]
Влияние неподеленной пары фосфора здесь не сказывается. [3]
Под влиянием неподеленной пары связывающие пары сближаются, что ведет к уменьшению угла между связями. [4]
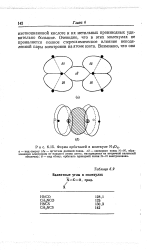 |
Форма орбиталей в молекуле N204. [5] |
Очевидно, что в этих молекулах не проявляется полное стереохимическое влияние неподеленной пары электронов на атоме азота. [6]
 |
Схема строения молекулы СО2.| Электрические моменты а некоторых полярных молекул. [7] |
Большое расхождение в общих электрических моментах молекул NH3 и NF3 можно объяснить влиянием неподеленной пары электронов в орбитали атома азота, которое в одном случае увеличивает общий результат, а в другом случае уменьшает, так как знаки электрических моментов N - - Н и N - F - обратны. [8]
 |
Структурные параметры молекул типа NO2X.| Структурные параметры молекул XNO и XNCO. [9] |
Углы XNO всегда имеют значения, меньшие 120; очевидно, это связано с влиянием неподеленной пары электронов. Однако ее длина совпадает с длиной связи в оксиде азота ( см. с. Итак, хотя мы считаем, что в молекуле имеется одинарная связь X - iN и двойная N-О, на самом деле часть электронной плотности перенесена со связи X-N на N-О. В то же время, связи N-F в молекуле цис 2р2 ( 31) имеют обычную для одинарных связей длину, а расстояние N-N соответствует длине двойной связи. [10]
В каждой связи N - Н ионный характер и размеры оказывают противоположное влияние; если первая из этих величин больше, то каждый из диполей отдельных связей имеет отрицательный конец у азота. В случае NF3 влияние размеров несущественно, так как оба атома имеют примерно одинаковые размеры, но и ионный характер и вклад неподеленных пар фтора ( если они находятся на частично гибридных зр3 - орбитах) вместе создают диполи связей N-F с отрицательным концом у фтора. Таким образом, в NF3 влияние неподеленной пары у азота направлено в сторону, противоположную моментам связей N-F, и не удивительно, что NF3 имеет очень маленький дипольный момент. [11]
Теоретическая модель, выдвинутая Дункеном и Поплом [37], представлена на фиг. Связывающие электроны группы ОН расположены на расстоянии 0 584 А от центра атома кислорода, это расстояние почти совпадает с атомным радиусом кислорода ( табл. 3.5), равным 0 6 А. Важной чертой модели Дункена и Попла является то обстоятельство, что она показывает влияние неподеленной пары электронов на величину дипольного электрического момента молекулы. [12]
Столь же сильное влияние на величину и направление дипольного момента могут оказать неподеленные электронные пары в трех - и четырехатомиых ге-тероядерных молекулах. Примером последних может служить пирамидальная молекула аммиака МНз. Если в молекуле BF3 в образовании связей принимают участие 2s -, 2px -, и 2ру - орбитали атома бора ( - гибридизация), определяющие ее плоскостное строение, то в молекуле аммиака заняты три взаимно перпендикулярные 2 / 7-орбитали, сильно возмущенные влиянием неподеленной пары 25-электронов. [13]
Как было показано, молекулы типа AX5L, в которых центральный атом имеет шесть электронных пар, одна из которых неподелена, имеют конфигурацию квадратной пирамиды, и неподеленная пара, как и следовало ожидать, вызывает удлинение экваториальных связей из-за увеличения отталкивания. Это имеет место, например для SbCljT, где длина экваториальной связи равна 2 62 А, а полярной - 2 36 А. Однако для двух других изученных молекул этого типа наблюдается обратное положение. Экваториальные и полярные длины связей для BrF5 и SbFf равны соответственно 1 68; 1 79 и 2 02; 2 08 А. Следовательно, для молекул этого типа в настоящее время не может быть предсказано влияние неподеленной пары на длину связей. [14]
Как было показано, молекулы типа AXbL, в которых центральный атом имеет шесть электронных пар, одна из которых неподелена, имеют конфигурацию квадратной пирамиды, и неподеленная пара, как и следовало ожидать, вызывает удлинение экваториальных связей из-за увеличения отталкивания. Это имеет место, например для SbCljT, где длина экваториальной связи равна 2 62 А, а полярной - 2 36 А. Однако для двух других изученных молекул этого типа наблюдается обратное положение. Экваториальные и полярные длины связей для BrF5 и 5ЬРГ равны соответственно 1 68; 1 79 и 2 02; 2 08 А. Следовательно, для молекул этого типа в настоящее время не может быть предсказано влияние неподеленной пары на длину связей. [15]
Страницы: 1 2