Влияние - разбавление
Cтраница 1
Влияние разбавления ил гидролиз проследим на следующем опыте. [1]
Влияние разбавления 20 М LiCl различными количествами насыщенного раствора трихлорида лантана на коэффициент распределения америция ( III) показано [ в табл. 8.11. Анализируя данные этой таблицы, легко заметить, что анионный обмен - прекрасная основа для разделения америция и лантана. [2]
Влияние разбавления на гидролиз проследим на следующем опыте. К 1 мл воды добавим 3 капли раствора соли хлорида сурьмы SbCls. При разбавлении раствора увеличивается концентрация ионов воды Н и ОН -, и вследствие усиления гидролиза раствор приобретает молочный цвет. [3]
Влияние разбавления на степень ионизации электролитов видно также и из таблицы VIII-2 при сопоставлении величин а для нормальных и децинормальных растворов. [4]
Влияние разбавления на степень ионизации электролитов видно также и из таблицы 12 - 2 при сопоставлении величин а для нормальных и децинормальных растворов. [5]
Влияние разбавления подобных растворов на рН сравнительно невелико, поэтому они называются буферными. [6]
Исследовано влияние разбавления, дополнительного контакта воды со смолой, температуры и обесфеноливания сточных вод на их коррозийные свойства. [7]
Выясняют влияние разбавления раствора на диссоциацию комплекса: проводят разбавление раствора в п раз и увеличивают толщину поглощающего слоя в п раз. Если комплексное соединение устойчиво, значение А не изменяется. Однако при разбавлении возможен гидролиз данного соединения, тогда произведение cl изменяется. Для поддержания постоянного значения рН разбавление проводят буферным раствором. [9]
Выясняют влияние разбавления раствора на диссоциацию комплекса: проводят разбавление раствора в п раз и увеличивают толщину поглощающего слоя в п раз. Если комплексное соединение устойчиво, значение А не изменяется. Однако при разбавлении возможен гидролиз данного соединения, тогда произведение d изменяется. Для поддержания постоянного значения рН разбавление проводят буферным раствором. [11]
Что касается влияния разбавления, то оказалось, что для всех кислот и оснований, выделяющих на электродах водород и киспород, потенциал разложения не зависит от разбавления. Сюда относятся все кислоты, за исключением тех, потенциалы разложения которых ниже максимального. У последних потенциал разложения увеличивается с возрастающим разведением, пока, наконец, не достигнет максимального значения. [12]
Чтобы уменьшить влияние разбавления на поглощение, рекомендуется применять сравнительно концентрированный раствор реагента, используемого для титрования. [13]
 |
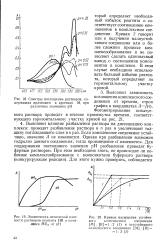
Кривые амперометрического титрования. [14] |
Чтобы уменьшить влияние разбавления раствора, применяют осадите ль с концентрацией в 10 - 20 раз большей, чем концентрация анализируемого раствора. [15]
Страницы: 1 2 3 4