Влияние - размер - молекула
Cтраница 2
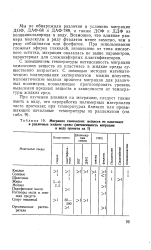 |
Миграция химических веществ из пластмасс. [16] |
Возможно, что влияние размера молекулы в ряду фталатов менее заметно, чем в ряду себацинатов или фосфатов. При использовании сложных эфиров гликолей, независимо от типа кислотного остатка, миграция оказалась не выше параметров, характерных для сложноэфирных пластификаторов. [17]
При этом углеродное вещество, полученное из легкого сырья, содержит в своей структуре больше водорода и частиц катализатора. Но, к сожалению, автором не было установлено влияние размеров молекул исходного сырья на геометрические параметры ( диаметр и длина) волокна. [18]
Далее необходимо выяснить, почему, собственно, УВ / УПТТ не зависит от В и каковы допустимые пределы варьирования структуры основания, в пределах которых это постоянство все еще соблюдается. Что касается первого вопроса, то некоторые вклады в ув и увн ( на-примзр, влияние размеров молекул, которые обсуждалось в разд. [20]
Произведение D % P не зависит существенно от давления при значениях Р от нескольких миллиметров ртутного столба до нет скольких десятков атмосфер, и уравнение ( X. Эта зависимость неприменима, однако, для высоких давлений, поскольку теория, на которой она основана, не учитывает влияния размера молекул на частоту молекулярных столкновений. Это влияние имеет важное значение при давлениях, вызывающих уплотнение упаковки молекул, например, в плотных жидкостях. [21]
Представления о структуре таких растворов, развитые А. Ю. Намиотом, основаны на двухструктурной модели воды. Предложено объяснение малой растворимости неполярных газов в воде, особенностей изменения объема воды при растворении в ней газов, а также влияния размеров молекул растворяемых газов на уменьшение их растворимости в результате добавления к воде солей. При давлениях 300 атм и температуре 0 С получены твердые растворы гелия, водорода и неона во льду. Показано, что газы, размеры молекул которых заметно превосходят размер пустот в решетке льда ( аргон), не образуют твердых растворов со льдом. [22]
Константа скорости диффузии представляет собой количество вещества, переносимое через единицу поверхности в единицу времени при градиенте концентрации, равном единице. При конвективной диффузии перенос вещества идет за счет энергии внешних сил. Влияние размера молекул, вязкости и других факторов, важных для внутренней диффузии, незначительно. [23]
При этом было замечено, что с уменьшением молекулярной массы углеводорода одного гомологического ряда происходит увеличение выхода углеродного вещества. Углеродное вещество, полученное из легкого сырья, содержит в своей структуре больше водорода и частиц катализатора. Но, к сожалению, автором не было установлено влияние размеров молекул исходного сырья на геометрические параметры ( диаметр и длина) волокна. Кроме того, основная часть исследований сводилась к получению целевого продукта - волокнистого углеродного вещества из доступных видов сырья, а возможности использования ресурсов газообразного сырья и утилизации образующегося в процессе водород - или олефинсодержащего газа не было уделено достаточного внимания. [24]
На первый взгляд может показаться, что эти экспериментальные факты и, дополнительно зависимость М2, Кр от размера диффундирующих молекул, противоречат соотношениям (4.3) и (4.12), согласно которым Мкр не зависит от природы диффузан-та. Однако это противоречие кажущееся. Формально зависимость Мкр от размера молекул диффузанта связана с влиянием размеров молекул на постоянную В, с одной стороны, и ограниченной точностью в определении D, с другой. [25]
В любом случае едва ли можно ожидать точного равенства адсорбционных объемов, поскольку полностью исключить мо-лекулярноситовой эффект не представляется возможным, даже если средняя ширина пор составляет несколько молекулярных диаметров. В адсорбентах, как правило, наблюдается распределение пор по размерам, и доля пор, доступных данным молекулам, будет тем меньше, чем больше размеры молекул. Фостер [1, 34] обнаружил, что большинство этих данных подчиняется измененному правилу Гурвича xs / p0 25 - - 0 0007 V, в котором поправка на молекулярный объем V ясно выражает влияние размеров молекул на значение предельных адсорбированных объемов. [26]
Он нашел, что подвижность на электрофореграмме у нитро -, нитрозо -, азо -, арилметановых и антрахиноновых красителей зависит от присутствия в молекуле полярных групп, например SOsH. Накопление полярных групп увеличивает подвижность красителя, тогда как значение RF при БХ уменьшается. Влияние размера молекулы красителя сказывается так же, как и при БХ. С увеличением сложности и размера молекулы красителя его подвижность в электрическом поле уменьшается. В разных электролитах по-разному проявляется склонность красителя к поляризации или диссоциации. [27]
Для изучения влияния функциональной группы ( карбоксильной, амино и гидрок-сильной) были выбраны алифатические углеводороды с трех -, семи - и девя-тиуглеродными цепями. Органические вещества, молекулы которых содержат большее число углерода в цепи, не могут быть показательными для оценки влияния функциональных групп, так как они совершенно нерастворимы. Для изучения влияния размера молекулы исследовали ароматические соединения, содержащие в кольце кислотные, гидроксильные и аминные функциональные группы. Поскольку известно, что адсорбция алифатических веществ возрастает с увеличением содержания углерода, поэтому параллельно испытывали элиЛятические ч яппмятические ппгяничегкие вещества с одинаковой молекулярной массой. Адсорбцию каждого изучаемого компонента оценивали при двух значениях рН: одно - выше, другое - ниже того, при котором наступает диссоциация. [28]
Результаты, полученные для близких по своим свойствам, но обладающих различным молекулярным весом соединений, свидетельствуют о наличии влияния ближайших молекул, образующих как бы замкнутую ячейку, в которой находятся свободные радикалы и возбужденные молекулы в момент их образования под действием излучения. Вероятность их выхода из этой ячейки понижается с увеличением размера молекулы, и поэтому увеличиваются шансы рекомбинации или дезактивации. Поэтому большие молекулы в меньшей степени распадаются при облучении, чем маленькие. Однако к такому объяснению влияния размера молекул на их устойчивость при облучении следует относиться с известной осторожностью. [29]
Положительная энтальпия переноса в газовую фазу главным образом обусловлена потерями энергии вандер-ваальсовых взаимодействий, происходящих в жидкости. Отрицательное изменение энтропии, приблизительно - 1 4 энтр. Дж / моль - К), при переносе метиленовой группы из инертной среды в воду намного меньше, чем для метана, что, вероятно, указывает лишь на небольшое дополнительное структурирование воды при увеличении размеров молекулы углеводорода. Интересно, что свободная энергия растворения в воде жидкой метиленовой группы почти полностью определяется свободной энергией переноса в газовую фазу, так что свободная энергия переноса из газовой фазы в воду практически не зависит от размера молекулы углеводорода, в связи с чем растворимость углеводородов в воде при постоянном давлении пара не зависит от размеров их молекул. Влияние размеров молекулы на перенос углеводорода в газовую фазу можно объяснить потерями энергии вандерваальсовых взаимодействий, что проявляется в энтальпии испарения; пренебрежимо малое изменение свободной энергии при переносе из газовой фазы в воду указывает на то, что вандерваальсовы взаимодействия с водой и дополнительное увеличение степени сцепления молекул воды, непосредственно примыкающих к молекуле растворенного вещества, компенсируются увеличением затрат энергии на образование полости для большей молекулы. [30]
Страницы: 1 2 3
