Влияние - растворитель
Cтраница 1
Влияние растворителей довольно полно изучено на реакциях гидрирования. Так, например, скорость гидрирования кретоновой кислоты ( реакция нулевого порядка) [9] в разных растворителях ( 1 г кислоты, 9 мл растворителя, 0 1 г Pt при 20 и взбалтывании) приведена в табл. 2, где К-скорость реакции, выраженная в миллилитрах поглощенного водорода в 1 мин. [1]
Влияние растворителя на положение равновесия химической реакции определяется разностью влияний на стандартные потенциалы исходных и конечных веществ. Существование солевого эффекта убедительно показывает, что влияние свойств среды на скорость реакции определяется разностью влияния на стандартные потенциалы реагентов и переходного состояния, причем влияние на переходное состояние в принципе не отличается от влияния на стабильную молекулу. Поэтому в случае как скорости, так и равновесия проблема влияния растворителя на реакционную способность сводится к вопросу о влиянии растворителя на стандартный потенциал растворенного вещества. Этот эффект относительно понятен, когда растворенное вещество является электролитом. [2]
Влияние растворителей на константы сополимеризации нельзя рассматривать независимо от применяемого противоиона. [3]
Влияние растворителя не ограничивается только сдвигом полос, но проявляется также в изменении их ширины и формы и, быть может вследствие этого, в изменении абсолютных и относительных интенсивностей максимумов полос. У хлорофилла отношение интенсивностей сине-фиолетовой и красной полос ссвгршенно различно в разных растворителях. [4]
Влияние растворителя на флуоресценцию хлорофилла получило новое объяснение после опытов Ливингстона, Ватсона и Мак-Ардла [85], которые мы опишем ниже. Эти опыты говорят о том, что влияние растворителя имеет двойственный характер. Повидимому, это связано с превращением хлорофилла из нефлуоресцирующей вст флуоресцирующую таутомерную форму. После того как флуоресценция активируется таким путем, ее спектр и интенсивность не зависят от природы активатора и определяются только природой самого растворителя. Другими словами, активируется ли флуоресценция хлорофилла в бензоле метанолом, пиперидином или водой, ее спектр и интенсивность характерны для бензола как среды. Если прибавлять все большие и большие количества активатора, то рано или поздно спектр начнет приближаться к тому виду, который характерен для самого активатора. [5]
 |
Положение полосы поглощения ацетона в зависимости от природы растворителя / 236. [6] |
Влияние растворителя обычно обусловлено ассоциацией молекул растворителя и ослаблением взаимодействия растворителя с растворенным веществом и различно для различных растворителей. Полярные растворяемые вещества сильнее реагируют на изменение природы растворителя, чем неполярные. [7]
Влияние растворителя или пластификатора на вязкоупру-гие свойства в переходной зоне может быть проанализировано с точки зрения его влияния на температурную зависимость О - т ( Т) и отдельно с точки зрения его влияния на абсолютные значения коэффициента трения и на форму вязко-упругих спектров. [8]
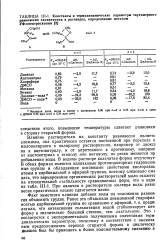 |
Константы и термодинамические параметры таутомерного равновесия оксикетонов в растворах, определенные методом УФ-спектроскопии. [9] |
Влияние растворителя на константу равновесия являете сложным, она практически остается постоянной при переходе о малополярного к полярному растворителю, например от диоксз на к ацетонитрилу, и от апротонного к протонному, наприме от ацетонитрила к этанолу или метанолу, но резко меняется пр добавлении воды. В водном растворе кольчатая форма отсутствуе - В обеих формах имеются одинаковые протонодонорные гидроксюп ные группы и обладающие основными свойствами кислороднь атомы в карбонильной и эфирной группах, поэтому следовало ОЖР дать, что варьирование органических растворителей мало скажете на относительной стабильности сравниваемых форм, что и видн из табл; III-1. При наличии в растворителе молекул воды равнс весие практически нацело сдвигается влево. [10]
Влияние растворителя на п - л - переход в карбонильном хромофоре. [11]
 |
Зависимость удельной константы скорости kf разложения диазоуксусного эфира от ост точной обменной емкости Е Н. [12] |
Влияние растворителя проявляется практически всегда и сводится к нескольким эффектам. [13]
 |
Зависимость ka от состава смесей растворителей. [14] |
Влияние растворителей в этом случае легко объяснимо с точки зрения поляризации связей С-Hg и Hg-Вг в молекулах реагентов. [15]
Страницы: 1 2 3 4