Влияние - побочная реакция
Cтраница 2
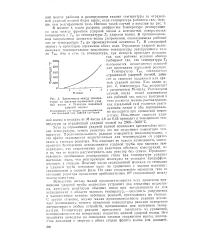 |
Зависимость между температурой за фронтом отраженной ударной волны и М - числом падающей ударной волны. [16] |
Вследствие весьма малой продолжительности всех процессов применение ударной трубы полностью устраняет два серьезных недостатка, присущих реакторам обычных типов при использовании их для исследований в области высоких температур, - опасность разрушения и маскирующее влияние побочных реакций, протекающих на стенках. С другой стороны, весьма малая продолжительность реакции исключает возможность точного измерения температуры реакции вследствие инерционности любых устройств, применяемых для измерения температуры. Температуру реакции приходится вычислять из уравнений, основывающихся на измеренных скоростях прямой ударной волны. [17]
Наконец, можно просто удлинить время пребывания реакционной массы в нитраторе до 1 5 - 2 ч и более и снизить температуру до 30 - 35 С. В этом случае влияние побочных реакций на выход нитросульфокислоты ничтожно мало. [18]
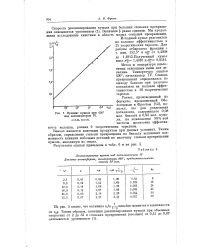 |
Крекинг кумола при 400 над катализатором IV. [19] |
Бензол является конечным продуктом при данных условиях. Таким образом, определение степени превращения по бензолу исключает возможность влияния побочных реакций на величину степени превращения кумола, находимую из опыта. [20]
При прочих равных условиях с понижением температуры процесса качество алкилата улучшается, скорость реакции понижается, расход серной кислоты падает. С повышением температуры, наоборот, расход серной кислоты возрастает, качество алкилата падает, скорость реакции повышается, увеличивается влияние побочных реакций. [21]
Эта формула имеет то достоинство, что она пригодна для любых значений р и для любых прибавленных индифферентных веществ - продуктов реакции или посторонних веществ. Формула (4.54) пригодна для начальных степеней превращения вдали от равновесия, что является ее достоинством в том отношении, что здесь меньше успевает сказаться влияние побочных реакций. [22]
На основании проведенных исследований сделано предположение, что данное уравнение может быть справедливо и для реакций науглераживания катализаторов. Для проверки этого предположения были проведены исследования образования углеродных отложений ( УО) при пиролизе газообразного углеводородного сырья ( метана, пропана, бутана) на железосодержащих катализаторах. С целью анализа влияния побочных реакций был исследован пиролиз пропилена и изобутилена на тех же катализаторах. [23]
Через несколько лет Дэвис и Лингейн [440] очень обстоятельно изучили поведение Ag2 как кулонометрического титранта и их заключение о возможностях применения последнего в аналитической химии оказалось менее пессимистическим. В охлаждаемом ( ниже 5 С) электролите с 0 1 М концентрацией AgNO3 и 5 М концентрацией HNO3 реакция восстановления Ag2 водой чрезвычайно замедляется и практически не вызывает ошибок. Если же генерирование Ag2 вести при комнатной температуре, то влияние побочной реакции становится все более заметным. В ходе титрования образовавшаяся окисная пленка может постепенно разрушиться, поэтому индикаторный электрод ( платина) сразу по окончании титрования погружают в указанный выше окисляющий раствор. [24]
Для определения воды, получающейся при сожжении, применяли субмикромодификации метода титрования по К - Фишеру, но достаточно четко выраженных конечных точек при этом достигнуть не удалось. Трудности прямых методов сожжения и титрования для определения углерода и водорода заставили обратить внимание на различные методы сплавления, в которых углерод превращается в цианиды, а не в двуокись углерода. Такие методы требовали более простой аппаратуры и техники, чем методы сожжения, однако в этих случаях возникали трудности, обусловленные влиянием побочных реакций и серьезных затруднений, связанных с недостаточной степенью чистоты различных реагентов. [25]
Расчет рН растворов электролитов и критериев их анализа может бьп осуществлен на основе математического моделирования протекающи процессов. Математическое описание должно отражать динамически равновесия в растворе между молекулами и ионами. Авторами этих работ описаны математические модел. Булатов [14] предложил использовать для расчетов так называемые условные константы устойчивости кислот и оснований, которые позволяют учитывать влияние побочных реакций на общее состояние равновесия. [26]
Фишеру, но достаточно четко выраженных конечных точек при этом достигнуть не удалось. Трудности прямых методов сожжения и титрования для определения углерода и водорода заставили обратить внимание на различные методы сплавления, в которых углерод превращается в цианиды, а не в двуокись углерода. Такие методы требовали более простой аппаратуры и техники, чем методы сожжения, однако в этих случаях возникали трудности, обусловленные влиянием побочных реакций и серьезных затруднений, связанных с недостаточной степенью чистоты различных реагентов. [27]
Проведена значительная работа с целью выяснения влияния перекиси водорода на вещества или процессы, имеющие биологическое значение. Эти исследования сильно отличаются друг от друга по глубине и методу. В некоторых случаях пользовались заведомо модельными системами, что давало возможность четко определить условия, однако результаты в отношении живых систем иногда имели лишь сомнительную ценность. Другие работы проведены с органическими веществами или in vivo, а поэтому они ближе к естественным условиям, по результаты с точки зрения влияния побочных реакций и ферментов получились менее определенными. [28]
В противоположность данным Нойеса с сотрудниками [ 333 - 3351 о быстром окислении двухвалентным серебром таких ионов, как Mn2, Cr3, As3 и Се3, Мейер и Свифт [338] нашли, что окисление указанных ионов в азотно - и хлорнокислых растворах протекает довольно медленно. Кроме того, ион Ag2 сравнительно легко восстанавливается водой, что также затрудняет возможность использования этого титранта в кулонометрии. Попытки применить биамперометрический и потенциометрический способы индикации конечной точки оказались практически безуспешными из-за очень медленного установления потенциала индикаторного электрода и неточности показаний амперометрической системы. Несколько лет спустя Дэвис и Лингейн [339] очень обстоятельно изучили поведение иона Ag2 как кулонометрического титранта, и их заключение о возможностях применения последнего в аналитической химии оказалось менее пессимистическим. В охлаждаемом ( ниже 5 С) электролите, в котором концентрация AgN03 и HN03 составляет соответственно 0 1 и 5 М, реакция восстановления иона Ag2 водой чрезвычайно замедляется и практически не вызывает ошибок. Если же генерирование иона Ag2 вести при комнатной температуре, то влияние побочной реакции становится все более заметным. В ходе титрования образовавшаяся окисная пленка может постепенно разрушиться, поэтому индикаторный электрод ( платина) сразу по окончании титрования погружают в указанный выше окисляющий раствор. Используемая при этом ячейка аналогична показанной на рис. 12, с той разницей, что площадь генераторного электрода значительно меньше, а индикаторный электрод сравнения ( насыщ. [29]
Кинетическая длина цепи / V определяется количеством превращений ( числом элементарных актов) на каждый случай инициирования цепи. Термическое разложение не является идеальным методом изучения реакций, происходящих с участием: радикалов, так как они протекают быстрее, чем первичная реакция с расщеплением связи С-С. Спорость и энергия активации всей реакции, таким образом, определяются в значительной степени первичной реакцией. Большая часть знаний о радикальных реакциях при термическом разложении углеводородов получена при изучении фотохимических и фотосенсибилизованпых реакций углеводородов, кетонов, меркуралкилов и альдегидов. В этих случаях энергия активации первичного расщепления не отражается на результатах кинетических анализов, и вся энергия активации является обычно простой функцией относительной энергии активации реакций различных радикалов. Возможно также прове дение работы при более низкой температуре, когда в значительной мере устраняется влияние побочных реакций. Таким образом, энергия активации и пространственные факторы в реакциях радикалов могут определяться независимо, ы о значении их можно судить-только по процессу чисто термического разложения. [30]
Страницы: 1 2