Влияние - внутримолекулярная водородная связь
Cтраница 1
Влияние внутримолекулярной водородной связи на реакционную способность обсуждается в обзоре: Садеков, Минкин, Луцкий. [1]
Влияние внутримолекулярной водородной связи на значения трКЕ аналогично эффекту сольватации. В зависимости от используемых систем растворителей образование внутримолекулярной водородной связи должно конкурировать с образованием водородной связи с растворителем. Поэтому молекулы, которые обнаруживают внутримолекулярную водородную связь в неполярных рас ворителях или в твердом состоянии, могут не показывать этой связи в водном или спиртовом растворе и, таким образом, могут давать значения рК, не указывающие на наличие данного эффекта. [2]
Влияние внутримолекулярных водородных связей на реакционную способность гидроксильных групп в реакции уретанообразования в меньшей степени отражено в литературе. В работе [5] развиваются взгляды, что наибольшей реакционной способностью в среде простых диметиловых эфиров обладают соединения, проявляющие склонность к образованию внутримолекулярной водородной связи. Авторы [5] объясняют это тем, что такие соединения проявляют меньшую склонность к образованию межмолску-лярной водородной связи между ОН-группой и эфирным кислородом растворителя, что приводит к уменьшению скорости реакции уретанообразоваиия. [3]
Влияние внутримолекулярной водородной связи на значения pKs аналогично эффекту сольватации. В зависимости от используемых систем растворителей образование внутримолекулярной водородной связи должно конкурировать с образованием водородной связи с растворителем. Поэтому молекулы, которые обнаруживают внутримолекулярную водородную связь в неполярных рас ворителях или в твердом состоянии, могут не показывать этой связи в водном или спиртовом растворе и, таким образом, могут давать значения рК, не указывающие на наличие данного эффекта. [4]
Влияние внутримолекулярных водородных связей на реакционную способность гидроксильных групп в реакции уретанообразования в меньшей степени отражено в литературе. В работе [5] развиваются взгляды, что наибольшей реакционной способностью в среде простых диметиловых эфиров обладают соединения, проявляющие склонность к образованию внутримолекулярной водородной связи. Авторы [5] объясняют это тем, что такие соединения проявляют меньшую склонность к образованию межмолекулярной водородной связи между ОН-группой и эфирным кислородом растворителя, что приводит к уменьшению скорости реакции уретанообразования. [5]
Другое исследование влияния внутримолекулярных водородных связей на скорость химических реакций проведено Кнорре и Эмануэлем [74], которые описали влияние водородных связей, хелатирования и растворителей на кинетику химических реакций. [6]
В некоторых случаях сказывается еще и влияние внутримолекулярной водородной связи, но очевидно, что, кроме этого, имеются сдвиги полос, зависящие от природы и положения заместителей. Иногда усиливаются также полосы колебаний связей СС кольца, так что они становятся даже сильнее, чем полосы карбонильных колебаний. Это происходит, например, в случае м - и л-окси-бензальдегидов. [7]
Возможно, что люминесценция этого соединения отсутствует вследствие влияния внутримолекулярной водородной связи. [8]
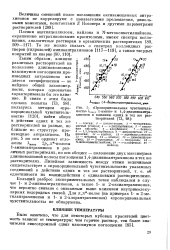 |
Пропорциональная чувствительность Ямакс 1-амино - и 1 4-диаминоантра. [9] |
Больший разброс экспериментальных точек наблюдался в случае 1 - й 2-аминоантрахинонов, а также 1 - и 2-оксиантрахинонов, что вероятно связано с описанным выше влиянием внутримолекулярных водородных связей. Для я я - полос ( на примерах 1 - и 2-ме-тилантрахинонов и 1 - и 2-хлорантрахинонов) пропорциональная чувствительность не обнаружена. [10]
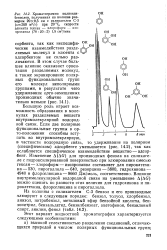 |
Хроматограмма полиокси-бензолов, полученная на колонне раз-мерой 20X0 3 см с силикагелем С-3 ( s 260 м2Д при 20 С, скорости элюента гексан - хлороформ - изо пропанол ( 78. 20. 2 1 5 см3 / мин. [11] |
Изменение A ( AG) для производных фенола на силикаге-ле с гидроксилированнои поверхностью при элюировании смесью гексан - хлороформ - изопропанол составляет для пирокатехина - 530, пирогаллола - 640, резорцина - 3800, гидрохинона - 4940 и флороглюцина - 8660 Дж / моль, соответственно. Влияние внутримолекулярной водородной связи на уменьшение A ( AG) можно оценить по разности этих величин для гидрохинона и пирокатехина, флороглюцина и пирогаллола. [12]
Скорость протонного обмена производных фенола с метанолом ( системы 9 - 11 в табл. 2.5) уменьшается при возрастании протонодонорной способности фенола. Этот ряд молекул представляет интерес для изучения влияния внутримолекулярной водородной связи ( в 2-хлорфеноле и 2 4 6-трихлорфено-ле) на скорость процесса обмена. Результаты работ [14, 38] свидетельствуют в пользу того, что образование внутримолекулярной водородной связи протоном группы АН сопровождается значительным уменьшением скорости протонного обмена. [13]
Правильнее говорить о том, что межмолекулярная водородная связь, существующая в конденсированных состояниях этих веществ, является причиной недостаточно низких значений их температур плавления. Это необходимо иметь в виду при обсуждении вопроса о влиянии внутримолекулярной водородной связи и на другие свойства веществ. [14]
Обратим внимание на интересные случаи разделения следующих двух пар изомеров. Во-первых, дезглюкохейротоксин адсорбируется на гидрофобной поверхности из полярного растворителя сильнее конваллятоксина, что связано с более выгодным расположением сахарного остатка по отношению к полярному элюенту во втором случае. Во-вторых, ланатозид В адсорбируется сильнее изомерного ему ланатозида С. Сильное увеличение Ki для ланатозида В связано, по-видимому, с рассмотренным выше гидрофобизую-щим влиянием внутримолекулярной водородной связи, в данном случае между гидроксильной группой в положении 16 [ см. формулу стерана (1.4) ] и лактонным кольцом. [15]
Страницы: 1