Влияние - растворенный электролит
Cтраница 1
Влияние растворенных электролитов на растворимость твердых и жидких неполярных веществ может быть описано теми же законами, что и для газов. [1]
Характер влияния растворенного электролита на растворимость газов в воде экспериментально изучил во второй половине XIX в. [2]
Харнед и Кук показали, что уравнение Дебая-Гюккеля учитывает влияние растворенных электролитов на величину K w в разбавленных растворах. [3]
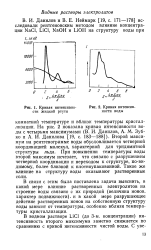 |
Кривая интенсивности жидкой ртути.| Кривая интенсивности воды. [4] |
В связи с этим была поставлена задача выяснить, в какой мере влияние растворенных электролитов на строение воды связано с их природой ( величина ионов, характер подвижности), и в какой мере разрушающее действие растворенных ионов на собственную структуру воды зависит от температуры, особенно вблизи температуры кристаллизации. [5]
В теории Подольского [135] была сделана попытка объяснить изменения коэффициента самодиффузии воды под влиянием растворенных электролитов. Эта теория исходит из теории диффузии Эйринга ( ср. По уравнению (3.1.59) расстояние К, покрываемое диффундирующей молекулой в одном элементарном акте ( активированный перескок), имеет важное значение в выражении для коэффициента диффузии. [6]
Применение метода изотопных и температурных эффектов гидратации позволяет при минимальном воздействии на изучаемую систему судить о происходящих под влиянием растворенного электролита структурных изменениях воды. При этом важно подчеркнуть, что наблюдаемые изотопные и температурные эффекты непосредственно связаны с ближним взаимодействием между частицами растворенного вещества и растворителя. [7]
Гидроокись Ре ( ОН) з может содержаться в поверхностных водах в виде коллоидного раствора, но под влиянием растворенных электролитов она коагулирует. [8]
В простейшем случае L определяется вычитанием удельной электропроводности чистого растворителя L0 из электропроводности раствора L. Если L0 не очень мало по сравнению с L, то необходимо учитывать влияние растворенного электролита на электропроводность растворителя. Например, если большая часть электропроводности растворителя обусловлена присутствием ионов, образовавшихся из растворенной углекислоты, то очевидно, что эта часть электропроводности значшельно уменьшится в присутствии сильной кислоты, например такой, как соляная. Таким образом, при вычислении L из экспериментальных значений L и L0 следует принимать во внимание как природу электролита, так и природу растворителя. [9]
В простейшем случае L определяется вычитанием удельной электропроводности чистого растворителя L0 из электропроводности раствора L. Если L0 не очень мало по сравнению с L, то необходимо учитывать влияние растворенного электролита на электропроводность растворителя. Например, если большая часть электропроводности растворителя обусловлена присутствием ионов, образовавшихся из растворенной углекислоты, то очевидно, что эта часть электропроводности значительно уменьшится в присутствии сильной кислоты, например такой, как соляная. Таким образом, при вычислении L из экспериментальных значений L и L0 следует принимать во внимание как природу электролита, так и природу растворителя. [10]
Мак-Колл и Дуглас [141] также указали, что сложное явление гидратации необходимо учитывать при рассмотрении соотношения между самодиффузией и структурными свойствами растворов. Среднее время жизни гидратной оболочки некоторых ионов составляет несколько часов, в то время как этот параметр для других ионов так мал, что релаксация не влияет на некоторые процессы. Модель, учитывающая, что ионы оказывают влияние не на все, а лишь на часть молекул воды, также является слишком упрощенной. В связи с влиянием растворенных электролитов на самодиффузию также следует указать, что, хотя концепцию гидратированных ионов можно с пользой применить при описании некоторых явлений, она в действительности слишком упрощает очень сложные эффекты. [11]
Это число зависит от размера молекулы неэлектролита и от степени разветвленно-сти ее неполярных групп. Оставшиеся неразорванныади водородные связи в результате упрочняются. Однако считают, что это упрочнение происходит не вследствие образования комплексов молекул воды под действием водородных связей, а главным образом вследствие вандерваальсовых взаимодействий между водой и неполярной частью растворенного неэлектролита. Далее предполагается, что взаимодействие между водой и неполярными группами растворенного вещества становится возможным вследствие существования определенных структурных зон или соответствующих им неполярных групп молекул, форма и размер которых облегчают вандерва-альсовы взаимодействия. Контакт с группами ОН в воде осуществляется наилучшим образом тогда, когда радиусы ван-дерваальсова взаимодействия для неполярной группы и для структурных зон воды равны между собой. При этом условии водородные связи групп ОН становятся линейными. Согласно этой картине, стабилизирующее действие неэлектролитов яа структуру воды связано главным образом с зависимостью взаимодействий между молекулами от их ориентации. При повышении температуры водородные связи постепенно деформируются, что приводит к повышению координационного числа и одновременному уменьшению числа структурных зон. В результате этого ослабляется влияние растворенных электролитов на структуру. [12]
Страницы: 1