Влияние - давление - кислород
Cтраница 2
Учитывая описанные особенности процесса растворения сульфида одновалентной меди, сначала было изучено влияние давления кислорода на скорость растворе -, ния ковеллина при 25 С, концентрации цианида 1 85Х Х10 - 2 моль / л и скорости вращения диска 128 об / мин. [16]
Методика выработана в многочисленных опытах с различными борорганическими веществами, ставившихся с задачами: выяснить оптимальную массу сжигаемого вещества и соответственно массу, форму и размеры чашечки для сожжений, выбрать лучший сорт стекла для изготовления ампул - контейнеров для сжигаемых образцов, предпочтительную форму ампул и расположение их в чашечке для сожжения, способ зажигания вещества, влияние давления кислорода в бомбе и пр. [17]
Оценка последней основы - Мммат. Влияние давления кислорода кает значительно быстрее, на скорость горения углерода. [18]
В зависимости от внешней газовой среды температура инкон-груентного плавления иттриево-железистого граната Y3Fe5012 различна. Специальное исследование влияния давления кислорода на температуру инконгруентного плавления Y3Fe8012 [7] показало, что с увеличением давления кислорода эта температура повышается и при давлении 100 атм. [19]
Эти немногие наблюдения иллюстрируют возможные эффекты, а также указывает на необходимость и достаточность адсорбционной модели, предложенной Мельником. Данные Хайланда и Мельника по влиянию давления кислорода иллюстрируют роль адсорбированного кислорода в явлении фотопроводимости. Из работы Хайланда можно, в частности, сделать вывод, что кислород влияет на процесс затухания медленной фотопроводимости. Чтобы наблюдаемые эффекты были обратимы, необходимо, чтобы кислород десорбировался при освещении образца. Адсорбированный кислород, став нейтральным атомом, десорбируется. [20]
Однако при более строгом подходе к изучению свойств ферритов не следует пренебрегать влиянием давления кислорода при синтезе и спекании. [21]
 |
Скорость адсорбции кислорода. [22] |
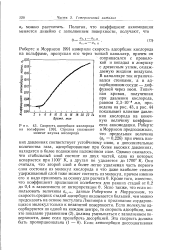
Типичная кривая, полученная при давлении кислорода, равном 2 3 - 10 - 8 мм, приведена на рис. 43, а рис. 44 показывает влияние давления кислорода на конечную величину коэффициента аккомодации. Роберте и Моррисон предположили, что предельная величина ( ас 0 226) при очень низких давлениях соответствует устойчивому слою, а дополнительные количества газа, адсорбированные при более высоких давлениях, находятся в более подвижном наложенном слое. Однако оказалось, что стабильный слой состоит из двух частей, одна из которых испаряется при 1100 К, а другая не удаляется до 1700 К. Ясно также, что если использовать величины аС) 00, данные Робертсом и Моррисоном, то скорость средних стадий адсорбции оказывается большей, чем можно предсказать на основе постулата Лэнгмюра о прилипании соударяющихся молекул только к незанятой поверхности. Если молекулы адсорбируются по одной на каждом центре, то скорость адсорбции, как это показано уравнением ( 2), должна уменьшаться с заполнением поверхности, даже если пренебречь десорбцией. [23]
При 450 С окисление тантала не зависит от давления в интервале изменения последнего от 4 до 100 мм рт. ст., что согласуется с вагаеровским механизмом. Как установили Каугилл и Отрийгар [234], при температурах 600 - 900 С и давлении кислорода от 1 до 760 мм рт. ст. скорость окисления возрастает по боль-шей части пропорционально квадратному корню из давления кислорода. Этой закономерности соответствует механизм окисления, рассматривавшийся нами на стр. В случае ниобия взаимосвязь между скоростью окисления и давлением довольно сложна [706] и трудно поддается истолкованию. Фаосел с сотрудниками определили при температурах 400 - 900 С влияние давления кислорода на окисление ниобия [241] и тантала [201] вплоть до 40 атм; в частности, они выявили зависящий от давления пик на кривой скорости окисления ниобия при 550 - 600 С. [24]
Страницы: 1 2