Влияние - парциальное давление
Cтраница 3
 |
Влияние температуры на выход этилена.| Пиролиз этана при 800. [31] |
Вследствие того, что при полузаводских испытаниях не был освещен вопрос о влиянии парциального давления, последний был изучен в лабораторных условиях. [32]
В большинстве экспериментальных данных парциальное давление воздуха было мало, примерно около 0 008 мм рт. ст. Для выяснения вопроса о влиянии парциального давления сухого воздуха на интенсивность испарения льда были проведены специальные опыты при общем неизменном давлении 0 7 мм рт. ст. Парциальное давление воздуха изменялось от 5 - 10 3 до 5 - 10 - 2 мм рт. ст. - в 10 раз. [33]
В большинстве экспериментальных данных парциальное давление воздуха было мало, примерно около 0 008 мм рт. ст. Для выяснения вопроса о влиянии парциального давления сухого воздуха на интенсивность испарения льда. [34]
При изучении каталитической реакции ( статическая объемно-метрическая установка о циркуляцией газовой фазы через раствор j / аОН для поглощения C0v) определено влияние парциальных давлений СО, С, природа лиганда, температура на стабильность и активность комплексов палладия. Показано что как стабиль - нооть, так и активность катализатора увеличиваются при уменьшении концентрации СО в реакционной газовой омеои. [35]
 |
Влияние температуры на растворимость сульфатов кальция и бария в воде. [36] |
Однако с уменьшением давления и температуры из раствора выпадает осадок СаСО3, ибо на направление реакции по схеме (V.15) в значительно большей степени, чем температура влияет парциальное давление углекислого газа. Влияние парциального давления СО2 на растворимость МСаСОз в воде дано ниже. [37]
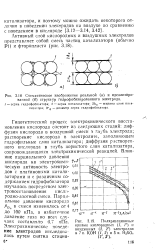 |
Схематическое изображение реальной ( о и идеализированной ( б структур гидрофобизированного электрода. [38] |
Гипотетический процесс электрохимического восстановления кислорода состоит из следующих стадий: диффузия кислорода в воздушной смеси в глубь электрода; растворение кислорода в электролите, заполняющем гидрофильные слои катализатора; диффузия растворенного кислорода в глубь пористого слоя катализатора, сопровождающаяся электрохимической реакцией. Влияние парциального давления кислорода на электрохими - f s ческую активность электро - V5 дов с платиновыми катали - 7 00 заторами и с различным содержанием гидрофобизатора) э5 изучалось посредством элек - 030 тровосстановления кислородно-азотной смеси. [39]
Значения степени черноты ег f ( t, pi) для углекислого газа приведены на фиг. Для водяного пара влияние парциального давления рНа0 несколько сильнее, чем /, поэтому значение ен о, найденное из фиг. [40]
Была установлена зависимость выхода изопентана от мольного отношения водород: н-пен-тан, рабочего давления, температуры и объемной скорости подачи н-пентана. Было изучено также влияние парциальных давлений н-пентана и водорода на скорость протекания реакции. [41]
Данные о давлении пара для этих систем, полученные приведенными выше исследователями, показаны графически на рис. 14.2 - 14.4. 14.3, основанный на опубликованных данных [4], дает основания для распространенного взгляда, что окись углерода абсорбируется в результате образования нестабильного комплексного соединения, содержащего 1 моль СО на 1 моль одновалентной меди. На рис. 14.4 показано влияние парциального давления окиси углерода на количество окиси углерода, абсорбированное растворами различного состава. На этой диаграмме представлены данные, полученные при одном значении температуры ( 20 С); однако на основании рис. 14.4, где показано влияние температуры на давление паров СО при различных концентрациях окиси углерода в типичном поглотительном растворе, можно определить показатели и при других значениях температуры. [42]
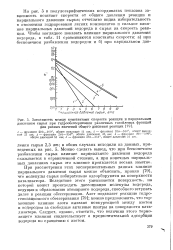 |
Зависимость между константами скорости реакции и парциальным давлением сырья при гидрообессеривании различных газойлевых фракций для разных значений общего давления реакции [ 791. [43] |
Можно сделать вывод, что при бесконечном разбавлении сырья влияние парциального давления водорода сказывается в ограниченной степени, а при конечных парциальных давлениях сырья это влияние проявляется весьма заметно. При рассмотрении этих экспериментальных данных влияние парциального давления сырья можно объяснить, приняв [79], что молекулы сырья избирательно адсорбируются на поверхности катализатора. Вследствие этого уменьшается поверхность, на которой может происходить диссоциация молекулы водорода, ведущая к образованию атомарного водорода способного вступать далее в реакции обессеривания. Азот подавляет реакцию гидро-генизационного обессеривания [79]; можно предположить, что тормозящее влияние азота вызвано конкуренцией между азотом и водородом за свободные активные центры на поверхности катализатора. Следует, однако, отметить, что величина этого тормозящего влияния свидетельствует о предпочтительной адсорбции водорода по сравнению с азотом. [44]
 |
Распределение предельных и непредельных углеводородов по числу атомов углерода в молекуле. [45] |
Страницы: 1 2 3 4 5