Влияние - общее давление
Cтраница 2
Когда для определения энтальпий сублимации используются данные о давлении пара, может оказаться необходимым учет влияния общего давления на равновесное давление пара твердого вещества. [16]
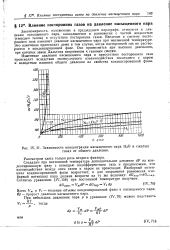 |
И - Зависимость концентрации насыщенного пара Н2О в сжатых газах от общего давления. [17] |
Изменение давления насыщенного пара в присутствии постороннего газа происходит вследствие молекулярного взааимодействия последнего с паром и вследствие влияния общего давления на свойства конденсированной фазы. [18]
Изменение давления насыщенного пара в присутствии постороннего газа происходит вследствие молекулярного взаимодействия последнего с паром и вследствие влияния общего давления на свойства конденсированной фазы. [19]
Термодинамическая формулировка закона Генри (VI.1) совпадает с первоначальной в условиях низких давлений, поскольку при таких давлениях парциальное давление приближается к летучести компонента, а влиянием общего давления на коэффициент Генри можно пренебречь. [20]
При повышенных температурах из-за роста давления пара воды резко увеличивается общее давление, что приводит к условиям, в которых газы нельзя считать идеальными, и следует учитывать влияние общего давления на коэффициент Генри. [21]
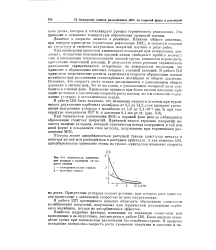 |
Зависимость концентрации углерода п молибдене от скорости откачки. [22] |
Влияние общего давления, при котором проводится термическое разложение МОС, и скорости откачки на структуру и свойства получаемых покрытий изучено в ряде работ. [23]
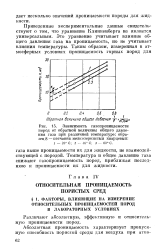 |
Зависимость газопроницаемости пород от обратной величины общего давления газа при различной температуре. образец 8 - песчаник мелкозернистый кварцевый. 1 - 20 С. 2 - 40 С. 3 - 60 С. [24] |
Приведенные экспериментальные данные свидетельствуют о том, что уравнение Клинкенберга не является универсальным. Это уравнение учитывает влияние общего давления газа на проницаемость, но не учитывает влияния температуры. [25]
 |
Распределение предельных и непредельных углеводородов по числу атомов углерода в молекуле. [26] |
Выражения для скорости первой реакции в ( 47), а также функций ( 50) и ( 51) выведены в работе [9] с использованием представлений о детальном механизме реакций. Эти уравнения оказались достаточно гибкими для описания влияния общего давления, а также для описания влияния парциальных давлений ( фугитивностей) СО, Н2, СО2 и Н2О на соответствующие скорости в широких пределах изменения указанных переменных. [27]
Следует остановиться на требуемой степени очистки нефтепродуктов от сероводорода. Однако при выборе предельной допускаемой концентрации сероводорода, для того чтобы учесть влияние общего давления в системе, удобно пользоваться величиной парциального давления HaS. Содержанию сероводорода в газовой фазе 0 1 % ( неопасному) при общем давлении 0 1 МПа соответствует парциальное давление HsS 0 0001 МПа. Эта величина и характеризует требуемую степень очистки нефтепродуктов от сероводорода для предотвращения водородного расслоения металла оборудования. [28]
Для каждой такой температуры существуют две строго определенных критических концентрации двуокиси азота, между которыми происходит немедленное воспламенение смеси водорода с кислородом, но выше и ниже которых наблюдается только крайне медленная реакция. Около 400 С нижняя критическая концентрация ( далее обозначаемая н.к.к.) имеет величину порядка 0 1 мм Hg, а верхняя критическая концентрация ( далее обозначаемая в.к.к.) есть величина порядка нескольких мм Hg. При постоянной температуре и составе смеси н.к.к. растет, а в.к.к. падает с возрастанием общего давления водорода и кислорода. Если общее давление поддерживается постоянным, в.к.к. понижается с ростом отношения парциального давления кислорода в смеси к парциальному давлению водорода; она понижается также благодаря присутствию азота. Влияние общего давления на н.к.к. с падением температуры становится менее отчетливым, в. В следующей таблице приведены значения критических концентраций для стехио-метрической смеси водорода с кислородом при различных температурах и давлениях. [29]
Для каждой такой температуры существуют две строго определенных критических концентрации двуокиси азота, между которыми происходит немедленное воспламенение смеси водорода с кислородом, по выше и ниже которых наблюдается только крайне медленная реакция. Около 40Э С нижняя критическая концентрация ( далее обозначаемая н.к.к.) имеет величину порядка 0 1 мм Hg, а верхняя критическая концентрация ( далее обозначаемая в.к.к.) есть величина порядка нескольких мм Hg. При постоянной температуре и составе смеси н.к.к. растет, а в.к.к. падает с возрастанием общего давления водорэда и кислорода. Если общее давление поддерживается постоянным, в.к.к. понижается с ростом отношения парциального давления кислорода в смеси к парциальному давлению водорода; она понижается также благодаря присутствию азота. Влияние общего давления на н.к.к. с падением температуры становится менее отчетливым, в. В следующей таблице приведены значения критических концентраций для стехио-метрической смеси водорода с кислородом при различных температурах и давлениях. [30]
Страницы: 1 2