Влияние - дейтерий
Cтраница 1
 |
Нитрование ароматических углеводородов борфторидом нитрония. [1] |
Влияние дейтерия в этих реакциях и характер изменения изотопного эффекта при переходе от л л-комплекса к комплексу с хлористым водородом и затем к комплексу с нитроний-катионом согласуются с предположением Халеви [19] о небольшой степени переноса заряда в л - л-комплексах. Более детально изотопные эффекты дейтерия здесь не рассматриваются, поэтому мы отсылаем читателя к прекрасной статье Халеви [21], посвященной этому вопросу. [2]
Влияние дейтерия на реакции между Np ( V) и Np ( III) и между Pu ( III) и О2 слишком мало, чтобы можно было принять механизм с переходом атома водорода. Небольшое замедление объясняется влиянием D2O на сольватацию реагирующих молекул. [3]
Во введении мы кратко коснулись влияния дейтерия на скорость отщепления других атомов водорода или дейтерия, связанных с тем же атомом углерода. В результате такого процесса образуется карбанион. [4]
Авторы работ [106] считают, что влияние дейтерия можно объяснить уменьшением константы кислотной диссоциации D2O2 по сравнению с константой Н202, так как k 2k K. Путем экстраполяции данных Гарни [107] было найдено, что Кт2о2 примерно в 4 2 раза меньше, чем Кн2о2 [ Ю8 ], что приблизительно соответствует наблюдаемому уменьшению константы скорости. [5]
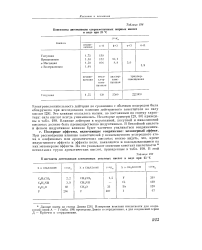 |
К онстанты диссоциации замещенных уксусных кислот в воде при 25 С. [6] |
Влияние дейтерия в муравьиной, уксусной и пивалиновой кислотах должно быть преимущественно индуктивным. В бензойной кислоте и феноле индуктивное влияние будет частично усиливаться сопряжением. [7]
В условиях опыта k мало изменялось с изменением ионной силы раствора, k уменьшалось с уменьшением ионной силы. Определено также влияние дейтерия на скорость реакции. [8]
Упомянем также данные Барлетта и Тэта [99] но определению отношения / CD / / CU для полимеризации аллилацетата с дейтерием в а-положение к аллкльной группе в присутствии перекиси бензоила. Рост скорости под влиянием дейтерия в а-положе-нии вызван увеличением средней длины полимеризационной цепи и связан с переносом а-водорода на стадии, заканчивающие ценную полимеризацию. [9]
 |
Зависимость константы. [10] |
Ожидалось, что замена водорода дейтерием сильно повлияет на наблюдаемую скорость при первой реакции, тогда как при второй влияние дейтерия должно быть незначительным. Полученные результаты ( табл. 5 - 7) показали, что скорость реакции в D2O в 1 7 раза больше, чем в обычной воде. Это увеличение скорости авторы объясняют тем, что значение константы равновесия (5.17) в тяжелой воде больше, чем в обычной. [11]
В первом механизме происходит переход кислорода в скоростьопределяющей реакции (2.26), во втором - переход водорода. По какому из этих двух механизмов в действительности идет реакция, невозможно определить на основании имеющегося опытного материала. Изучение влияния дейтерия на скорость реакции, очевидно, внесло бы некоторую ясность в этот вопрос, однако такое исследование не было предпринято. [12]
Это объясняется тем, что скоррсть образования продуктов определяется скоростью разрыва связи С - Н ( или С-D), а поскольку скорость разрыва связи С-D меньше, чем G - Н - связи, отщепление с участием СЮ2 - группы будет более медленным. В случае El-отщепления сохраняются те же аргументы, несмотря на то что в наиболее медленной стадии реакции связи С - Н или С-D непосредственно не затрагиваются. Однако стадии, на которых происходит образование конечного продукта, должны протекать с участием этих связей, и влияние дейтерия будет сказываться на распреде лении продуктов, как это описано для Е2 - отщепления. [13]
Для дициандиамида существует несколько структурных формул. Выбор между ними может быть сделан на основе наблюдения полос поглощения в инфракрасной области, нахождения характеристических частот. Однако для однозначного решения вопроса необходимо доказать, что в данном случае не происходит смещения частот, или, если смещение происходит, найти причину смещения. Для этого проводятся наблюдения дейтеро-замещенных и некоторых солей. Учитывая влияние дейтерия и металлов, можно однозначно решить вопрос о выборе той или другой структурной формулы. [14]
Подтверждение того, что-давление газообразного водорода может легко приводить к распространению трещи в высокопрочных сталях, указывает на то, что, вероятно, механизм разрушения не включает диффузию водорода в пустоты металла, где имеет место разрушающее давление газа. Следует принимать во внимание и предположение о том, что водород диффундирует в решетку непосредственно перед вершиной трещины и облегчает деформацию в этом месте [23], поскольку имеются доказательства того, что водород препятствует движению дислокаций. Остается, однако, неясным, понижает ли водород поверхностную энергию за счет адсорбции, или он, скапливаясь на расстоянии нескольких атомных слоев от вершины трещины, способствует снижению химического потенциала за счет упругих напряжений, тем самым понижая силу сцепления в решетке. Ориани [24] предпочитает последнее, поскольку это единственный механизм, который согласуется с наблюдениями влияния на распространение трещины небольших изменений в давлении газообразного водорода и замены дейтерия на водород. Значительное уменьшение давления газообразного водорода, окружающего образец с развивающейся трещиной при заданном значении коэффициента интенсивности напряжений, будет приостанавливать развитие трещины, но последующее увеличение давления от 1 6 кН / м2 до 22 кН / м2 будет достаточным для дальнейшего роста трещины; задержка роста трещины во времени была такой короткой, что даже в самом лучшем случае водород, внедряющийся в решетку за счет увеличения давления, мог продиф-фундировать не более, : чем на несколько атомных слоев. Аналогичное быстрое увеличение скорости развития трещины наблюдается при небольших изменениях прикладываемого катодного тока для мартенсит-но-стареющей стали в растворе хлористого натрия. Влияние дейтерия на уменьшение скорости хрупкого разрушения, по-видимому, не связано с различиями в кинетике транспорта двух изотопов, а обусловлено их разной растворимостью в искаженной решетке перед вершиной трещины. [15]
Страницы: 1