Структура - инсулин
Cтраница 1
Структура инсулина была определена Сэнджером ( разд. [1]
Структура инсулина достаточно консервативна. Аминокислотная последовательность инсулина человека и многих животных различается всего на 1 - 2 аминокислоты. У рыб по сравнению с животными В-цепь больше и содержит 32 аминокислотных остатка. [2]
 |
Расщепление кортикотропина свиньи различными протеиназами ( Stei. [3] |
При расшифровке структуры инсулина Сэнджером были использованы оба вида гидролиза - химический и энзимати-ческий. [4]
Вслед за установлением структуры инсулина и рибонуклеазы были расшифрованы аминокислотные последовательности еще нескольких белков, а именно лизоцима, белка оболочки вируса табачной мозаики, химотрип-синогена, трипсиногена, папаина, миоглобина, гемоглобина, цитохрома с. [5]
Сколько цистронов кодируют в ДНК структуру инсулина. [6]
Инсулин животных имеет несколько иную первичную структуру, отличающуюся от структуры инсулина человека. Инсулин, вводимый путем инъекций при заболевании человека диабетом, - это инсулин свиньи и крупного рогатого скота. Инсулин крупного рогатого скота имеет ту же цепь Б, что и инсулин свиньи, но цепь А отличается от цепи А инсулина человека тем, что имеет в положении 8 - 10 аминокислотные остатки Ala Ser-Val вместо Thr-Ser-Ile. Инсулин слона имеет такую же цепь Б, как и инсулин человека, но цепь А отличается тем, что в положениях 9 и 10 вместо Ser-Ile находятся Gly-Val. [7]
Протеолитическое расщепление проинсулина in vivo приводит к инсулину, стабильность которого обеспечивается энтропийным вкладом его нативной системы связей S-S ( разд. Лабильность структуры инсулина имеет, по-видимому, физиологическое значение [ 444J, поскольку скорость инактивации является фактором, контролирующим степень и продолжительность действия гормона. [8]
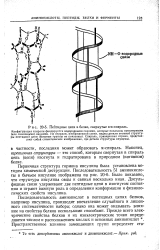 |
Пептидные цепи в белке, свернутые в а-спираль. [9] |
Первичная структура гормона инсулина была установлена методом химической деструкции. Было показано, что структура инсулина овцы и свиньи несколько иная. Дисуль-фидные связи удерживают две пептидные цепи в изогнутом состоянии и играют важную роль в определении конформации и физиологических свойств инсулина. [10]
Вначале, на волне революционных событий в физике, возникла биофизика, значительно окрепшая уже в предвоенный период. Конец этого этапа был ознаменован и резкой активизацией исследований в генетике. Однако наиболее серьезное наступление началось в начале 50 - х годов, когда возникли молекулярная биология, рождение которой часто отождествляется с открытием двойной спирали ДНК, а также биоорганическая химия, первые победы которой по праву связывают с установлением структуры инсулина и синтезом первого пептидного гормона - окситоцина. [11]
Первый влияет на протекание родов у женщин и образование молока, второй контролирует водный обмен в организме. Инсулин, вырабатываемый поджелудочной железой, контролирует метаболизм сахаридов, и его недостаток приводит к диабету. Инсулин состоит из двух цепей, одна из которых содержит 21, а другая - 30 аминокислотных остатков. Структура инсулина точно известна, и он был синтезирован. Другой пептидный гормон, адренокортикотропный гормон ( АКТГ), регулирует синтез стероидных гормонов в коре надпочечников, а соматотропин контролирует рост. Оба этих гормона вырабатываются передней долей гипофиза. К гормонам, образующимся в пищеварительном тракте, относятся, например, секретин и гастрин. [12]
Почти полностью определена первичная структура рибонуклеазы. Недавно было опубликовано сообщение о расшифровке структуры белка вируса табачной мозаики. Структуры инсулина, рибонуклеазы и белка вируса табачной мозаики показаны на фиг. Единственным хорошо исследованным растительным ферментом является папаин. Папаин содержит шесть остатков цистеина, один из которых обладает высокой реакционной способностью, но в его молекуле нет дисульфидных мостиков. [13]
 |
Кристаллический инсулин ( получен по методу Штальмана. [14] |
Эти аминокислоты твфйзуют две полипептидные цепи, так как удалось обнаружить два N-концевых аминокислотных остатка ( фенил-аланин и глицин) и два С-концевых аминокислотных остатка ( аланин и аспарагин), причем полипептидные цепи соединяются друг с другом поперечными мостиками, образованными дисульфидными группами. В настоящее время последовательность соединения аминокислот в молекуле инсулина полностью расшифрована. Схематически структуру инсулина ( для молекулярного веса 6000) можно изобразить следующим образом ( см. также стр. [15]
Страницы: 1 2