Структура - миоглобин
Cтраница 1
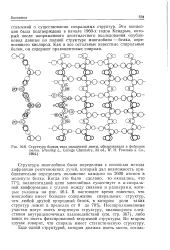 |
Структура белков типа складчатой ленты, обнаруженная в фиброине шелка. ( Pauling L, College Chemistry, 3d ed., W. H. Freeman a. Co., 1964. [1] |
Структура миоглобина была определена с помощью метода дифракции рентгеновских лучей, который дал возможность приблизительно определить положение каждого из 2600 атомов в молекуле белка. Неспирализованные участки могут иметь вторичную структуру, являющуюся следствием внутрицепочечных взаимодействий ( см. стр. Во втором случае говорят, что спираль имеет статистическую структуру. [2]
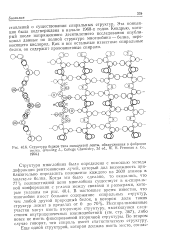 |
Структура белков типа складчатой ленты, обнаруженная в фиброине шелка. ( Pauling L., College Chemistry, 3d ed., W. H. Freeman a. Co., 1964. [3] |
Структура миоглобина была определена с помощью метода дифракции рентгеновских лучей, который дал возможность приблизительно определить положение каждого из 2600 атомов в молекуле белка. Нсспирализованные участки могут иметь вторичную структуру, являющуюся следствием внутрицепочечных взаимодействий ( см. стр. Во втором случае говорят, что спираль имеет статистическую структуру. [4]
 |
Структура миоглобииа. [5] |
Рассмотрим структуру миоглобина и гемоглобина. Эти важные белки были первыми, детально изученными методом рент-геноструктурного анализа; о них будет идти речь и в дальнейшем ( см. гл. [6]
Что же стабилизирует структуры миоглобина и изогнутого полипептида на рис. 40.1, который напоминает изображение рибонуклеазы - природного кеспирализовапиого белка. По аналогии с а-спиралью или вторичной структурой типа складчатой ленты можно предположить, что фиксированная конформация белка поддерживается за счет водородных связей. [7]
Что же стабилизирует структуры миоглобина и изогнутого полипептида на рис. 40.1, который напоминает изображение рибонуклеазы - природного неспирализованного белка. По аналогии с а-спиралью или вторичной структурой типа складчатой ленты можно предположить, что фиксированная конформация белка поддерживается за счет водородных связей. [8]
Апомиоглобин имеет богатую спиралями глобулярную структуру, подобную структуре миоглобина. В отличие от неустойчивой напоминающей кокон оболочки гема в цитохроме с в гемоглобине полость гема образована из жестких стабильных а-спиралей. Группа гема здесь не является основным элементом, определяющим укладку цепи: апомиоглобин, например, образует третичную структуру и в отсутствие простетических групп ( гл. Более мягкие структурные требования к взаимодействию гема и белка в гемоглобинах отражает также тот факт, что для членов семейства глобинов [277, 634] инвариантна только общая картина неполярных контактов гема. Структурно эквивалентные положения у них заняты различными аминокислотными остатками. [9]
Остается выяснить, насколько эти обобщения, полученные при изучении структуры миоглобина, справедливы в отношении других белков. [10]
Помимо наличия относительно длинных спиральных участков существует еще одна выдающаяся особенность структур миоглобина и гемоглобина, которая заключается в полном отсутствии регулярности, что, вероятно, связано с отсутствием порядка в последовательности боковых цепей. Поскольку для каждой боковой, цепи предпочтительно соседство других определенных боковых, цепей ( см. раздел 7), можно надеяться, что только нерегулярная структура будет удовлетворять этим условиям. [11]
Как уже указывалось, третичная структура обеих пар цепей гемоглобина лошади аналогична структуре миоглобина. Подобную же структуру имеют цепи миоглобина тюленя и гемоглобина быка. Интересно сравнить аминокислотные последовательности этих цепей, обладающих аналогичной третичной структурой. На первый взгляд они не имеют ничего общего, поскольку их аминокислотный состав совершенно различен. Однако анализ показал, что в а - и р-цепях гемоглобина и в молекулах мио-глобинов некоторые аминокислотные остатки занимают идентичное положение в глобуле. Например, в местах изгиба в этих цепях часто находятся остатки пролина, в местах сближения между сегментами спирали - остатки глицина; образование водородных связей между сегментами происходит через остатки тирозина; с железом тема связан гистидин. В этом и состоит основное сходство трех структур. Последовательность остатков в спиральных участках может быть совсем различной, но для стабилизации этой структуры существенно, чтобы внутри глобулы находились неполярные остатки. [12]
 |
Модель молекулы гемоглобина. [13] |
Общий вид молекулы изображен на рис. 10.9. Примечательно, что, как легко различить, каждая субъединица в основном идентична структуре миоглобина ( см. также разд. [14]
К составным белкам, а конкретно к металлопротеидам, относятся близкие по своей структуре миоглобин и гемоглобин. Эти глобулярные белки содержат небелковую компоненту, пигмент крови - гем ( разд. Степень окисления железа при таком переносе не изменяется, и оно остается двухвалентным. Структура миоглобина более простая, чем структура гемоглобина. В растительном мире ( Rhizobium) известен гемопротеид - леггемоглобин, который по своей структуре близок к миоглобину. [15]
Страницы: 1 2