Структура - молекула - бензол
Cтраница 1
Структура молекулы бензола выражается следующей схемой, где обозначают электроны, которые попеременно в количестве 6 или 8 связаны с атомами углерода. Если пара электронов разделена между двумя атомами, то по предположению авторов электроны за исключением случая с водородом квантуются в соответствии с полем между атомами, и действие их зарядов распределено между атомами в отношении положительных зарядов их двух ядер. [1]
 |
Распределение т-электронной плотности в пиридине ( расчеты по методу МО ab initio. [2] |
Родство структур молекул бензола и пиридина распространяется также и на другие шестичленные сопряженные циклические системы, содержащие более одного атома азота в кольце. [3]
 |
Структурные формулы бензола. [4] |
Если мы попытаемся представить структуру молекулы бензола с помощью обычных структурных формул, следует так видоизменить вкладываемый в них смысл, чтобы это позволило отразить важнейшие свойства данного вещества. Простая шестиугольная структура с чередующимися двойными связями, изображенная на рис. 27.4, а, недостаточна для такой цели. Но в комбинации с аналогичной структурой, показанной на рис. 27.4 6, в которой двойные связи расположены по-иному, она позволяет выразить представление о делокализации электронов с помощью такого понятия, как резонанс. Делокализованные связи представляют также кругом, изображенным внутри шестиугольника, как это показано на рис. 27.4 в. И все же следует признать, что в нашем распоряжении нет простой структурной формулы, удовлетворительно описывающей свойства молекулы бензола. В этом и заключается смысл понятия резонанса - отдельные структуры, которые мы записываем для этой молекулы, порознь друг от друга бессмысленны. Подлинная структура бензола представляет собой комбинацию двух ( или большего числа) эквивалентных структур. До сих пор не найдено статической структурной формулы, которая бы удовлетворительно описывала бензол. Поэтому молекула бензола называется резонансным гибридом. Следует подчеркнуть, что понятие резонанса представляет собой модель, предназначенную для объяснения определенных экспериментальных данных и теоретических результатов. Следовательно, представление о резонансе является лишь попыткой описать истинное строение некоторых молекул типа бензола. [5]
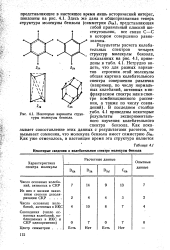 |
Некоторые варианты структуры молекулы бензола.| Некоторые сведения о колебательном спектре молекулы бензола. [6] |
Результаты расчета колебательных спектров четырех структур молекулы бензола -, показанных на рис. 4.1, приведены в табл. 4.1. Нетрудно видеть, что для разных вариантов строения. [7]
Эти факты совместимы только с циклической шестичленной структурой молекулы бензола. [8]
Рассмотрим в качестве примера вопрос о структуре молекулы бензола с точки зрения молекулярной спектроскопии. Известно, что бензол относится к числу соединений, структура которых в течение многих лет изучалась самыми разнообразными методами, причем были предложены различные варианты строения этой молекулы. [9]
Примеры эйдетической интуиции - наглядное представление о структуре молекулы бензола, возникшее у Кекуле, или наглядное представление о строении атома, созданное Резерфордом. Эти представления не сводятся к простому воспроизведению данных непосредственного чувственного опыта и формируются с помощью понятий. Примеры концептуальной интуиции - возникновение понятия о кватернионах у Гамильтона или понятия о нейтрино у Паули. Эти понятия возникали не путем последовательного логического рассуждения ( хотя данный процесс предварял открытие), а скачкообразно; большое значение при их формировании имело комбинирование соответствующих чувственных образов ( комбинаторная игра образными элементами мышления, по выражению А. [10]
Но строение молекул пиридина очень близко к структуре молекул бензола. Поэтому можно допустить, что атомные поляризации пиридина и бензола приблизительно одинаковы. Атомная поляризация бензола РА известна. Группа NO2 молекулы нитробензола имеет большую подвижность, чем группы СН в бензольном кольце. [11]
ОК) - В течение последних лет много работ посвящено решению проблемы структуры молекулы бензола. В только что приведенных формулах изображены попеременно двойные и простые связи, но такая простая формула по ряду причин является неудовлетворительной. Атомы водорода в С6НЙ могут быть замещены галоидами или такими группами, как СН, NO, и многими другими. Кроме того, существование только одного однозамещенного производного показывает, что все шесть атомов углерода эквивалентны друг другу. [12]
 |
Гидрирование стирола ( 1, аллилбензола ( 2, бензаль-дегида ( 3 на ( Pd ftAu - катализаторах на АЬО3 в эта-иолоне при 25 С. [13] |
При гидрировании бензола в указанных мягких условиях ( Pd rtAu) - катализаторы оказались практически неактивными. По-видимому, это связано е особенностью структуры молекулы бензола, наличием сопряженной системы двойных связей, я-электроны которых делокализованы. Как известно [8, 9], механизм жидкофазного гидрирования в первую оче редь зависит от степени адсорбции водорода и ненасыщенных соединений и энергии связи их с поверхностью катализатора. Слабая адсорбционная способность прочного бензольного ядра, а также значительная энергия связи водорода с поверхностью катализатора ( - 238 кДж / моль) [9, 10] приводит к резкому замедлению процесса гидрирования. Наличие С О-группы вблизи бензольного ядра повышает скорость реак ции. Однако, как видно из рис. 2 - 3, бензальдегид гидрируется со зна чительно меньшей скоростью, чем стирол и аллилбензол. [14]
 |
Гидрирование стирола ( 1, аллилбензола ( 2, бензаль-дегида ( 3 на ( Pd яАи - катализаторах на АЬОз в эта-нолоне при 25 С. [15] |
Страницы: 1 2