Структура - молекула - вода
Cтраница 2
Удовлетворительное совпадение значения наблюдаемых основных частот D20 со значениями частот, получаемых с помощью изотопических соотношений из спектра частот Н20, подтверждает правильность нашего предположения о структуре молекулы воды. [16]
Измерения диполъного момента ( см. § 12.9) часто дают существенные качественные сведения о строении молекулы [9], в частности, по льзуясь этими измерениями, можно сразу установить изогнутую структуру молекулы воды. Естественно ожидать, что атомы водорода должны быть положительно заряжены по сравнению с атомом кислорода, образуя таким образом диполь. Однако если бы молекула имела линейное строение, то эти диполи взаимно погашались бы; так, атомы водорода были бы ориентированы в прямо противоположных направлениях. С другой стороны, при изогнутой структуре это уже не должно иметь места. [17]
Он начинает с утверждения, что Н - связь, как известно, в своей основе электростатична по природе и что модель, использованная Бауэром и Мага [172], неудовлетворительна в свете более новых сведений о структуре молекулы воды. [18]
Структура молекулы воды схематически изображена на стр. [19]
Хотя углы межъядерных связей Y-С-X в органических соединениях в основном равны 109 5; 120; 180 ( что отражает sp3 -, sp2 - и sp - гибридизацию соответственно), отталкивание между парами валентных электронов достаточно велико для того, чтобы вызвать отклонения в идеальной геометрии связен. Рассмотрим структуру молекулы воды. [20]
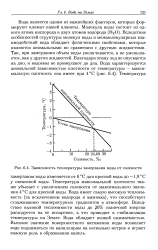 |
Зависимость температуры замерзания воды от солености. [21] |
Вода является одним из важнейших факторов, которые формируют климат нашей планеты. Вследствие особенностей структуры молекул воды и межмолекулярных взаимодействий вода обладает физическими свойствами, которые являются аномальными по сравнению с другими жидкостями. Так, при замерзании объем воды увеличивается, а не уменьшается, как у других жидкостей. Благодаря этому лед не опускается на дно, и водоемы не промерзают до дна. [22]
Ионы же, находящиеся в ней, в зависимости от их свойств лишь усиливают или ослабляют проявляемый эффект. При этом происходит изменение структуры молекул воды и растворов в целом. [23]
От иона Н3О, образующегося при этом процессе, протон может перейти к другой молекуле воды, и таким образом положительный заряд будет переноситься за короткий промежуток времени на значительное расстояние. На основании известных данных о структуре молекулы воды было подсчитано, что от иона Н3О к молекуле воды протон должен пройти расстояние 0 86 - 10 - 8 см, причем в результате положительный заряд перемещается на 3ЫО-8 см. Таким образом, в этом случае электропроводность будет значительно больше, чем электропроводность, обусловленная только нормальным механизмом проводимости. [24]
Почему же для жидкой воды характерно столь сильное взаимное притяжение молекул. Ответ на этот вопрос вытекает из самой структуры молекулы воды. Каждый из двух атомов водорода ( в молекуле воды) объединяет свой электрон с одним из электронов атома кислорода. Более электроотрицательный атом кислорода стремится притянуть электроны атомов водорода; поэтому на ядрах обоих атомов водорода ( протонах) локализуются частичные положительные заряды. Хотя молекула воды в целом электрически нейтральна, ее частичные отрицательный и положительный заряды пространственно разделены, что приводит к возникновению у нее электрического дипольного момента. Такой тип электростатического притяжения называется водородной связью. [26]
Как отмечалось ранее, другим методом, позволяющим изучать взаимодействие воды с ионами, является непосредственно исследование кристаллогидратов. Этот класс соединений довольно обширен и поэтому позволяет изучать изменение структуры молекул воды, составляющих ближайшее окружение катиона, при образовании ею водородной связи с самыми различными ионами, и, в первую очередь, с анионами. [27]
 |
Модельное изображение процесса отжатия из цементного. [28] |
Следовательно, действие поля сил от внешнего давления прежде всего должно способствовать восстановлению структуры молекулы воды - снижению вязкости ее до вязкости обычной воды, так как только при этом условии может отжиматься жидкость из цементного геля. [29]
Так как сдвиг полосы тесно связан с увеличением дипольного момента ОН-групп молекул воды в поле катиона, то это означает, что он непосредственно связан с взаимодействием катиона и воды типа взаимодействия ион - индуцированный диполь, или, точнее, с взаимодействием катиона и индуцированным им диполем. Ион-дипольное взаимодействие не может существенно изменять положение полосы, так как оно не меняет структуры молекул воды. [30]
Страницы: 1 2 3
