Структура - неорганическое вещество
Cтраница 1
Структуры неорганических веществ, Гостехтеориздат. [1]
Структуры неорганических веществ, Гостехтеорет-издат. [2]
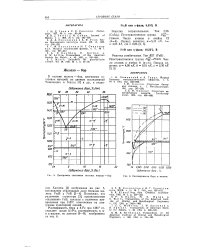 |
Диаграмма состояния системы железо - бор.| Растворимость бора в железе. [3] |
Структуры неорганических веществ, Гостехтеоо-издат, 1950, стр. [4]
 |
Фазовая диаграмма системы ванадий - углерод. [5] |
Структуры неорганических веществ, Гостехтеориэдат, 1950, стр. [6]
Рассмотрим структуру типичных неорганических веществ. На рис. 1 приведена кристаллическая структура хлорида натрия. Атомы одного вида находятся в вершинах куба и в центрах каждой грани, противоположно поляризованные атомы также расположены по вершинам куба и в центрах каждой его грани. Только второй куб смещен от первого на кратчайшее расстояние между атомами натрия и хлора. В целом хлорид натрия образует гранецентрированную кубическую решетку. В этой решетке каждый атом натрия окружен ближайшими шестью атомами хлора, и Наоборот. [7]
Рассмотрим структуру типичных неорганических веществ. На рис. 1 приведена кристаллическая решетка хлорида натрия. [8]
Рассмотрим структуру типичных неорганических веществ. На рис. 1 приведена кристаллическая структура хлорида натрия. Атомы одного вида находятся в вершинах куба и в центрах каждой грани, противоположно поляризованные атомы также расположены по вершинам куба и в центрах каждой его грани. Только второй куб смещен от первого на кратчайшее расстояние между атомами натрия и хлора. В целом хлорид натрия образует гранецентрированную кубическую решетку. В этой решетке каждый атом натрия окружен ближайшими шестью атомами хлора, и наоборот. [9]
Рассмотрим структуру типичных неорганических веществ. [10]
Часть третья Регистр исследований структур неорганических веществ является результатом ответственной и чрезвычайно трудоемкой работы автора, о содержании которой подробно говорится в вводном параграфе к III части. [11]
Киига представляет собой обзор структур неорганических веществ, систематизированных на основе периодической системы элементов и освещаемых с позиций современной теории. [12]
 |
Кристаллическая решетка NaCl Светлые шары - ионы Na. темные - ионы Cl. [13] |
Структурные типы NaCl и CsCl являются довольно широко распространенными среди структур неорганических веществ, в частности, все галиды щелочных металлов имеют структуры, принадлежащие к этим типам. В обычных условиях решетку типа хлорида цезия имеют CsCl, CsBr и Csl, остальные галиды щелочных металлов имеют структуру типа NaCl. [14]
Надо надеяться, что в ближайшее десятилетие проводимые советскими учимыми исследования структур неорганических веществ не только более равномерно охватят периодическую систему, но и позволят правильно интерпретировать ряд проблем теории валентности и, в окончательном итоге, будут гораздо более широко использованы также в неорганической химии. [15]
Страницы: 1 2