Структура - возбужденное состояние
Cтраница 1
Структура возбужденного состояния 1 3-диенов также Имеет знатге-ние для чис / гРанс ИЗомрризации. [1]
Хорошо, если нам удастся найти простые правила для предсказания структур возбужденных состояний, такие, например, как правило, данное выше для случая, когда к молекуле в основном состоянии добавляются электроны. Молекулы в возбужденном состоянии отмечены звездочкой. [2]
Есть несколько молекул, для которых не составляет проблемы понять структуру возбужденного состояния с точки зрения теории валентных связей. Например, для этилена, имеющего только два л-электрона, возбужденное состояние можно описать лишь через ионные структуры, которые в теории валентных связей обычно опускают. [3]
Описанная выше структура электронных оболочек отдельных атомов в невозбужденном состоянии позволяет понять и структуру возбужденных состояний атомов различных групп, периодической системы. [4]
Сравнительный анализ этих эффектов, проведенный в работе [31], на примере ряда широко используемых способов ограничения атомных статсумм показывают, что они существенно индивидуальны и зависят от структуры возбужденных состояний комплексной частицы. [5]
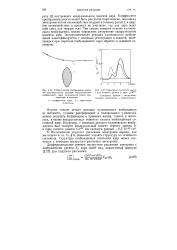
Поглощение света в видимой и ультрафиолетовой областях приводит к изменению электронной энергии молекул, связанному с возбуждением электронов, приводящим к переходу их со стабильных орбиталей на нестабильные. Для большинства таких изменений невозможно точно изобразить структуру возбужденного состояния с помощью обычных связей, поскольку возбужденный электрон не находится на нормальной связывающей орбитали. Обычно оказывается невозможным разрешить получающиеся в результате полосы поглощения в такой степени, чтобы можно было увидеть тонкую структуру, обусловленную колебательно-вращательными переходами. Вследствие этого полосы поглощения, связанные с электронным возбуждением, оказываются сравнительно широкими. [6]
Эти два вопроса очень тесно связаны, но, к сожалению, для них трудно найти простое объяснение. Затруднения возникают вследствие того, что нельзя выразить сколько-нибудь точно структуру возбужденных состояний молекулы с помощью обычных валентных схем. Однако из многих возможных схем спаривания, которые могут быть написаны для бутадиена ( три из них - XIX, XX и XXI - приведены ниже), только одна - XIX - имеет достаточно низкую энергию для того, чтобы вносить основной вклад в нормальное состояние бутадиена. [7]
Эти два вопроса очень тесно связаны, но, к сожалению, для них трудно найти простое объяснение. Затруднения возникают вследствие того, что нельзя выразить сколько-нибудь точно структуру возбужденных состояний молекулы с помощью обычных валентных схем. Однако из многих возможных схем спаривания, которые могут быть написаны для бутадиена ( три из них - XIX, XX и XXI - приведены ниже), только одна - XIX - - имеет достаточно низкую энергию для того, чтобы вносить основной вклад в нормальное состояние бутадиена. [8]
Эти два вопроса очень тесно связаны, но, к сожалению, для них трудно найти простое объяснение. Затруднения возникают вследствие того, что нельзя выразить сколько-нибудь точно структуру возбужденных состояний молекулы с помощью обычных валентных схем. Однако из многих возможных схем спаривания, которые могут быть написаны для бутадиена ( три из них - XIX, XX и XXI - приведены ниже), только одна - XIX - имеет достаточно низкую энергию для того, чтобы вносить основной вклад в нормальное состояние бутадиена. [9]
II, § 6, позволяет изучать структуру их основного состояния. Структура возбужденных состояний ядер может изучаться с помощью неупругого рассеяния электронов. [11]
Положение, аналогичное рассмотренному для этилена, обычно имеет место во всех других типах молекул. Основное состояние часто можно изобразить довольно точно с помощью одной структуры, а возбужденные состояния почти всегда требуют учета резонанса между несколькими структурами. Действительно, часто структуры возбужденных состояний сами по себе таковы, что их вообще нельзя описать с помощью общепринятых символов. Этому не следует удивляться, так как эти символы были разработаны химиками-органиками, которые интересовались изображением молекул в их химически обычных основных состояниях и не касались спектроскопических вопросов. Но если ограничиться рассмотрением только нескольких наиболее стабильных состояний из бесчисленного множества возбужденных состояний, то можно часто удовлетворительно представить их в терминах резонанса между несколькими структурами обычных типов. [12]
Таким образом, в очень короткий отрезок временя ( 10-в с), необходимый для возбуждения, расположение ядер в молекуле не меняется, так же как не меняется спин электрона. Однако после возбуждения эти изменения могут очень быстро произойти. Новая геометрия минимальной энергии связана со структурой возбужденного состояния, и молекула быстро принимает эту геометрию благодаря колебательным процессам. Между молекулами в возбужденном состоянии, обладающими более высокой, чем минимальная, колебательной энергией, и растворителем устанавливается термическое равновесие. Иногда химические реакции возбужденной молекулы протекают быстрее по сравнению с колебательной релаксацией, но в растворе это встречается редко. [13]
Страницы: 1