Структура - тридимит
Cтраница 3
В структуре кристобалита имеется кубическая плотнейшая укладка слоев [ Si2O5 ], а тридимита - гексагональная плотней-шая укладка. Расстояния Si-О, О-О и Si-Si в них одинаковь: для ближайших соседей, но несколько отличаются для более далеких атомов. Расчеты энергии связи для обоих типов peuieTOh показали, что при структуре кристобалита имеет место минимум энергии, а при структуре тридимита - максимум. Поэтому структура кристобалита оказывается более стойкой и, помимо прочю причин, получается легче при кристаллизации кремнеземистогс стекла. [31]
Отметим еще основание Миллона [ NHg2 ] OH и его соли, структуру которых можно рассматривать как производную структуры окиси кремния, где атомы кремния замещены атомами азота, а атомы кислорода - атомами ртути. Поскольку ртуть обладает сильной склонностью к образованию двух связей под углом 180 ( sp - гибридизация), то атомы ртути располагаются на середине линии, соединяющей два атома азота. Так как при этом атомы ртути имеют большие размеры ( радиус st; 1 4 А), то они раздвигают решетку так, что образуются большие пустоты, в которые могут внедряться крупные анионы. Структуру кристобалита имеет нитрат основания Миллона [ NHg2 ] NO3, из которого путем анионного обмена можно получить другие аналогичные соединения с той же структурой. Галогениды [ NHg2lHal большей частью обладают структурой тридимита, поскольку она имеет большие пустоты, необходимые для внедрения ионов галогенов. [32]
Отметим еще основание Миллона [ NHg2 ] OH и его соли, структуру которых можно рассматривать как производную структуры окиси кремния, где атомы кремния замещены атомами азота, а атомы кислорода - атомами ртути. Поскольку ртуть обладает сильной склонностью к образованию двух связей под углом 180 ( sp - гибридизация), то атомы ртути располагаются на середине линии, соединяющей два атома азота. Так как при этом атомы ртути имеют большие размеры ( радиус 1 4 А), то они раздвигают решетку так, что образуются большие пустоты, в которые могут внедряться крупные анионы. Структуру кристобалита имеет нитрат основания Миллона [ NHg2 ] NO3, из которого путем анионного обмена можно получить другие аналогичные соединения с той же структурой. Галогениды [ NHg2 ] Hal большей частью обладают структурой тридимита, поскольку она имеет большие пустоты, необходимые для внедрения ионов галогенов. [33]
Кристаллическая структура льда подобна структуре одной из модификаций кремнезема - тридимита. Предполагается, что при плавлении льда внутри температурного интервала от 0 до 4 С совершается переход от структуры тридими-та к другой, более плотной тетраздрической модификации кремнезема - кварцу. Следует учитывать, что в жидкости вследствие наложения поступательного ( или точнее трансляционного) движения на колебательное могут существовать лишь квазикристаллические статистические образования, представляющие собой некоторые аналоги соответствующих кристаллических структур. Максимальная плотность воды при 4 С объясняется наложением эффекта уплотнения ( связанного с переходом от структуры тридимита к структуре кварца) на эффект температурного расширения. Дальнейшее повышение температуры уменьшает упорядоченность в распределении частиц жидкости и вызывает переход воды в аморфное состояние. При температурах, близких к критической температуре воды, невозможно обнаружить проявления каких-либо элементов квазикристалличности. [34]
Кристаллическая структура льда подобна структуре одной из модификаций кремнезема - тридимита. Предполагается, что при плавлении льда внутри температурного интервала от 0 до 4 С совершается переход от структуры тридимита к другой, более плотной тетраэдрической модификации кремнезема - кварцу. Следует учитывать, что в жидкости вследствие наложения поступательного ( или точнее трансляционного) движения на колебательное могут существовать лишь квазикристаллические статистические образования, представляющие собой некоторые аналоги соответствующих кристаллических структур. Максимальная плотность воды при 4 С объясняется наложением эффекта уплотнения ( связанного с переходом от структуры тридимита к структуре кварца) на эффект температурного расширения. Дальнейшее повышение температуры уменьшает упорядоченность в распределении частиц жидкости и вызывает переход воды в аморфное состояние. При температурах, близких к критической температуре воды, невозможно обнаружить проявления каких-либо элементов квазикристалличности. [35]
Рентгенографические исследования воды показали, что вода имеет псевдокристаллическое строение. Молекулы воды обладают подвижностью, но в каждый момент времени имеют определенную ориентировку, временно группируясь на отдельных участках в правильную кристаллическую решетку. Происходит непрерывный процесс образования кристаллической решетки в одних участках и разрушения ее в других. При комнатной температуре структура образующейся решетки напоминает структуру кварца, по мере охлаждения она переходит в структуру тридимита, которой обладает лед. [36]
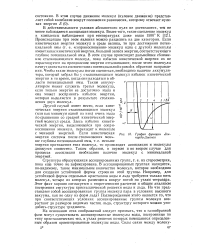 |
График функции нарда - Джонса. [37] |
В ассоциированных группах находится, по-видимому, такое минимальное количество молекул, которое необходимо для создания устойчивой формы строения этой группы. Например, для устойчивой формы отдельных кристаллов воды и льда требуется только пять молекул, четыре из которых размещены вокруг пятой: по углам тетраэдра. Этот факт хорошо согласуется с теоретическим расчетом и общим анализом построения структуры кристаллической решетки воды и льда. Но что представляет собой ассоциированная группа молекул пара в условиях высокого вакуума, как не одну из форм льда. Подтверждением этого является то, что при соответствующих условиях ассоциированные группы молекул возрастают до размеров видимых частиц льда, структуру которого можно уподобить структуре тридимита. [38]
Стевелс [14] объясняет это тем, что стеклообразный кремнезем имеет кристобалитоподобную структуру, так что для образования зародышей кристобалита требуется наименее существенная перестройка структуры. Даже при температурах ниже 1470 возникновение и рост кристаллов кристобалита происходят значительно быстрее, чем последующее превращение кристобалита в тридимит. Однако содержащиеся в кремнеземе примеси оказывают на него заметное влияние. При расстекловыва-нии ( 1220) кристаллы тридимита образовались в стеклах, содержащих LJ2O, Na2O и КгО, в то время как во всех других стеклах образовался кристобалит. Таким путем Стевелс подтвердил, что только окислы щелочных металлов оказывают каталитическое действие на превращение кристобалит-тридимит. Однако, если мы учтем мнение Флерке относительно стабильности тридимита, наблюдения Стевелса можно объяснить иначе. Стевелс, безусловно, прав, утверждая, что окислы щелочных металлов оказывают ускоряющее действие на фазовые превращения кремнезема, но более вероятно, что это объясняется способностью окислов щелочных металлов стабилизировать структуры тридимита. [39]
Страницы: 1 2 3