Структура - реагирующая частица
Cтраница 1
Структура реагирующей частицы достаточно полно отражена координатой 7 частицы углерода. [1]
Наличие данных о структуре реагирующей частицы стильбазо и состоянии иона галлия позволяет высказать предположение о строении внутрикомплексного соединения, образующегося в данных условиях. [2]
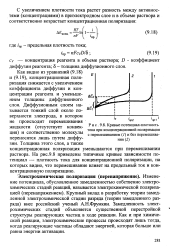 |
Кривые потенциал-плотность тока при концентрационной поляризации с перемешиванием ( 7 и без перемешивания ( 2. [3] |
Замедленность электрохимических стадий объясняется существенной перестройкой структуры реагирующих частиц в ходе реакции. Как и при химической реакции, электрохимические процессы происходят лишь тогда, когда реагирующие частицы обладают энергией, которая больше или равна энергии активации. [4]
 |
Зависимость электрохимической поляриза ции электрода от lg (. [5] |
Замедленность электрохимических стадий объясняется существенной перестройкой структуры реагирующих частиц в ходе реакции. Как и при химической реакции, электрохимические процессы происходят лишь тогда, когда реагирующие частицы обладают энергией, которая выше среднего уровня энергии молекул. Разность между энергией реагирующей частицы и средней энергией молекулы называется энергией активации. Частицы, энергия которых больше или равна энергии активации, называются активными. Только активные частицы способны к эффективному взаимодействию на электроде. Скорость электрохимических реакций, как и химических реакций, может быть увеличена повышением температуры и применением катализатора. При повышении температуры растет доля активных молекул, при применении катализатора снижается энергия активации. [6]
Замедленность электрохимических стадий объясняется существенной перестройкой структуры реагирующих частиц в ходе реакции. Как и при химической реакции, электрохимические процессы происходят лишь тогда, когда реагирующие частицы обладают энергией, которая больше или равна энергии активации. [7]
 |
Диаграмма потенциальной энергии эндотермической реакции образования. [8] |
Значения р лежат между 0 и 1 и зависят от структуры реагирующих частиц. [9]
 |
Стерические факторы и энергии активации газофазных реакций. [10] |
Стерическнй фактор для различных реакций варьирует в широких пределах; с усложнением структуры реагирующих частиц и увеличением роли ограничений по симметрии орбиталей фактор Р уменьшается. [11]
Исследование реакций замещения с участием стабильных радикалов позволяет установить некоторые связи между реакционной способностью и структурой реагирующих частиц, выяснить влияние л-комплексов, водородных связей и других факторов на кинетику радикальных реакций. [12]
Чтобы сделать анализ смеси двух компонентов, прежде всего необходимо найти такую реакционную систему, в которой наблюдалось бы достаточное различие в скоростях реакций с участием того и другого компонента. При выборе подходящей реакции и условий ее проведения для данной пары веществ принимаются во внимание особенности механизма реакций и влияние структуры реагирующих частиц на их реакционную способность. В области физической, органической и неорганической химии достигнуты огромные успехи в решении этих проблем. Тем не менее в настоящее время еще невозможно теоретически предсказать скорости реакций с такой точностью, которая позволила бы использовать этот расчет при выборе реакций для анализа. Обсуждение этой обширной области исследований выходит за рамки вопросов, рассматриваемых в этой книге. [13]
 |
Константы скорости к и энергии активации АЕ реакции роста цепи. [14] |
Образующиеся при взаимодействии излучения с мономером горячие частицы взаимодействуют друг с другом и со средой за время порядка 0 1 мксек ( 10 - 7 сек), после чего в системе устанавливается стационарная концентрация свободных катионов, к-рые и являются активными частицами процесса. Кроме того, кр для свободных катионов примерно в 50 раз ( стирол) больше, чем для свободных анионов. Это связано со структурой реагирующих частиц: свободный катион имеет незанятые низко расположенные энерге-тич. [15]
Страницы: 1 2