Электронная структура - элемент
Cтраница 1
Электронные структуры элементов, представленные в табл. 2, присущи изолированным или свободным атомам, у которых орбитали имеют дискретные значения энергии. Однако при сближении атомов элемента значения энергии внешних орбиталей не остаются дискретными, а размываются в определенный интервал энергий, известный под названием энергетической зоны ( см. гл. Когда атомы какого-либо элемента приводятся в очень тесное соприкосновение, как, например, в кристалле, то энергетические зоны, связанные с различными орбиталями, могут оказаться настолько широкими, что при этом некоторые из них будут перекрываться, в результате чего возможно образование гибридных орбиталей. Эти гибридные орбитали вносят определенный вклад в силы межатомного взаимодействия в кристалле. [1]
Электронные структуры элементов, представленные в табл. 1.1, присущи изолированным или свободным атомам, в которых различные типы орбиталей имеют дискретные значения энергии. [2]
Электронные структуры элементов, представленные в табл. 2, присущи изолированным или свободным атомам, у которых орбитали имеют дискретные значения энергии. Однако при сближении атомов элемента значения энергии внешних орбиталей не остаются дискретными, а размываются в определенный интервал энергий, известный под названием энергетической зоны ( см. гл. Когда атомы какого-либо элемента приводятся в очень тесное соприкосновение, как, например, в кристалле, то энергетические зоны, связанные с различными орбиталями, могут оказаться настолько широкими, что при этом некоторые из них будут перекрываться, в результате чего возможно образование гибридных орбиталей. Например, ns - и np - орбитали могут в результате гибридизации давать sp - гибридные орбитали, a ns -, пр-и ( и - 1) й-орбитали могут образовывать spd - гибридные орбитали. Эти гибридные орбитали вносят определенный вклад в силы межатомного взаимодействия в кристалле. [3]
Электронные структуры элементов Ilia, IVa, Va, и Via групп, соответствующие диаграмме энергетических уровней ( рис. 5.6), приведены в табл. 19.7. Все эти элементы имеют один или два электрона на s - op - битали внешней оболочки. Кроме того, у этих элементов имеется два, три, четыре или пять электронов на d - орбиталях предшествующей оболочки. Предполагается, и это показано на рис. 5.6, что самые тяжелые элементы рассматриваемых групп - торий, протактиний, уран и нептуний - имеют дополнительно от двух до пяти электронов соответственно а 5 / - подоболочке, а не на 6й - подоболочке. [4]
Электронные структуры элементов I, II, III и IV групп приведены в табл. 5.5. Распределение электронов по орбиталям в этой таблице точно такое же, как и на схеме электронных уровней ( рис. 5.11) с одним исключением: нормальное состояние атома лантана соответствует, по данным, полученным при изучении спектра лантана, наличию в этом атоме одного электрона на 5 -орбитали, а не на 4 / - орбитали, как показано на схеме энергетических уровней. [5]
Электронные структуры элементов пятого периода подчиняются закономерности, описанной выше для элементов четвертого периода. После заполнения 4й - подоболочки происходит заполнение уровней 5s и 5р в ряду элементов серебро - кадмий и индий - ксенон, которые входят в подгруппы IB - ПВ и IIIB - 0 соответственно. [6]
Электронные структуры элементов пятого периода подчиняются закономерности, описанной выше для элементов четвертого периода. У рубидия и стронция заполняются 5 -орбитали О-обо-лочкй, а затем следует вторая группа переходных металлов от иттрия до палладия, так как энергия 4с2 - орбиталей Л - оболочки оказывается значительно ниже энергии Ebs. После заполнения 4й - подоболочки происходит заполнение уровней 5s и 5р в ряду элементов серебро - кадмий и индий - ксенон, которые входят в подгруппы IB - IIB и IIIB - 0 соответственно. [7]
Рассмотрим электронную структуру элементов нижнего ряда четвертого периода от. [8]
Сложнее развиваются электронные структуры элементов VI периода. Затем у гафния и других элементов четного ряда, а также у золота и ртути заполняется электронами подуровень Ы предпоследнего слоя. [9]
Сложнее развиваются электронные структуры элементов VI периода. Затем у гафния и других элементов четного ряда, а также у золота и ртути, заполняется электронами подуровень 5d предпоследнего слоя. [10]
В табл. 16 приведена электронная структура элементов титана, циркония и гафния. [11]
В табл. 39 приводится электронная структура элементов главной подгруппы III группы. [12]
Правило Гунда позволяет проследить за электронными структурами элементов, которые образуются в результате последовательного добавления в электронное окружение ядра одного электрона за другим. Построение следует так называемому принципу надстройки. [13]
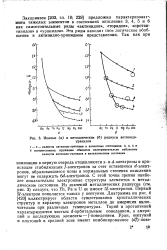 |
Ионные ( а и металлические ( б радиусы актинидо. [14] |
С этой точки зрения наиболее показательны электронные структуры элементов в металлическом состоянии. Из значений металлических радиусов ( см. рис. 3) следует, что Th, Ра и U не имеют 5 / - электронов. Первый Sf-электрон появляется только у нептуния. Диаграмма на рис. 4 [420] иллюстрирует области существования кристаллических структур и характер электронов металлов до америция включительно при различных температурах. Торий и протактиний характеризуются чистым rf - орбитальным поведением, а америций и последующие элементы - / - поведением. [15]
Страницы: 1 2 3