Кристаллическая структура - металл
Cтраница 2
Особенностью кристаллической структуры металлов являются большие координационные числа ( 8 - 12), свидетельствующие о большой плотности упаковки в кристаллических ячейках. [16]
В кристаллической структуре металлов или других проводников существуют относительно подвижные электроны. [17]
Действительно, кристаллическая структура металлов весьма сходна со структурой ионных соединений, построенных по принципу плотной упаковки, например, анионов в анионной подрешетке. Как это характерно для ионных соединений ( с ненаправленной и ненасыщаемой связью), координационное число атомов металла во всех наиболее часто встречающихся структурных типах является высокой величиной. [18]
Характерной особенностью кристаллических структур металлов является то, что электроны могут свободно перемещаться в объе-ме металла. Следствием свободного перемещения электронов является непрозрачность металлов, металлический блеск и высокая электрическая проводимость. При образовании связей между атомами металлов ( металлической связи) электроны оказываются принадлежащими всем атомам кристалла, т.е. они находятся не на атом - ных, а на молекулярных орбиталях. [19]
Характерной особенностью кристаллических структур металлов является то, что электроны могут свободно перемещаться в объеме металла. Следствием свободного перемещения элек - - тронов является непрозрачность металлов, металлический блеск и высокая электрическая проводимость. [20]
Различия в кристаллической структуре металлов определяют их физико-механические свойства. [21]
Однако в кристаллической структуре металла связь между атомами не может быть ионной или валентной. Ионы металла, расположенные в узлах решетки, имеют одноименные электрические заряды, а число валентных электронов явно недостаточно для образования двухзлек-тронной связи каждого атома со всеми окружающими его соседями. Поэтому приходится предположить, что при сближении атомов металла и образовании кристаллической решетки слабо связанные валентные электроны обслуживают уже не один определенный канал связи, как это было в рассмотренной выше двухатомной молекуле, а принимают участие в образовании сил притяжения между многими атомами. Валентные электроны, покинувшие свои места в атомах, становятся общими ( коллективными) для всех атомов. [22]
В одних случаях кристаллическая структура металла видна только при сильном увеличении, а в других можно установить глазом даже форму кристаллов. Такие металлы, как висмут, сурьма, легко образуют крупные кристаллы. На изломах палочек из цинка и олова хорошо видно кристаллическое строение этих металлов. [23]
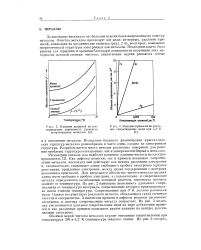 |
Влияние примесей на температурную зависимость удельного сопротивления металлов.| Влияние примесей на удельное сопротивление меди при 4 2 К. [24] |
Вследствие большого разнообразия кристаллических структур металлов разнообразна и часто очень сложна их электронная структура. Разрабатывается много методов различных измерений для решения проблемы структуры электронных зон и поверхностей Ферми в металлах. [25]
Прочность связи в кристаллической структуре металла характеризуется энтальпией атомизации, которая меняется от 61.4 кДж / моль у Hg до 850 кДж / моль у W. Максимальная энтальпия атомизации характерна для металлов рядов Nb-Ru и Hf-Ir. Относящиеся к ним металлы отличаются высокими температурами плавления и большой механической прочностью. [26]
Удаления окислов и выявления кристаллической структуры металла достигают травлением его в кислотах или щелочах. Однако поверхность металла, как правило, бывает загрязнена маслом 1ИЛИ жиром и не смачивается при взаимодействии с травильным ipacTBopoM, поэтому процессу травления должен предшествовать процесс удаления жиров и масел с поверхности изделий. Этот процесс условно принято называть обезжириванием. [27]
В таком целенаправленном изменении кристаллической структуры металлов состоит один из основных принципов легирования. [28]
Дискретный характер контакта и неоднородность кристаллической структуры металлов способствуют отрыву и закреплению на поверхности стружки относительно крупных частиц инструмента. [29]
Рентгеновский анализ служит для изучения кристаллической структуры металлов. Этот метод основан на дифракции рентгеновских лучей рядами атомов кристаллической решетки. Рентгеновские лучи представляют собой электромагнитные волны с длиной волны 0 0005 - 0 2 нм. Благодаря малой длине волны эти лучи возбуждают электроны атомов или ионов, находящихся в узлах кристаллической решетки. Поэтому атомы и ионы сами становятся источниками электромагнитных колебаний. Лучи, рассеянные отдельными атомами или ионами, взаимодействуют ( интерферируют) между собой. Вследствие упорядоченного расположения атомов в кристалле интерференция рассеянного излучения происходит таким образом, что в одних направлениях колебания усиливаются, в других ослабляются и гасятся. Возникающая интерференционная картина может быть истолкована как отражение лучей от отдельных кристаллографических плоскостей, подчиняющееся уравнению Вуль-фа - Брегга. [30]
Страницы: 1 2 3 4 5