Кристаллическая структура - соединение
Cтраница 2
Кристаллические структуры соединений переходных металлов с азотом и углеродом можно просто описать как плотнейшие ( или близкие к ним) упаковки металлических атомов, в междоузлия которых внедрены небольшие атомы неметаллов. В большинстве структур отсутствуют заметные локализованные взаимодействия углерод-углерод или азот-азот, характерные для органических соединений. Важными характеристиками карбидов и нитридов являются взаимодействие металл-неметалл и геометрия междоузлия. Атомы углерода и азота обычно располагаются в октаэдрических междоузлиях или в центре тригональных призм. На рис. 7 представлены типы междоузлий в гцк -, оцк -, гпу - или простой гексагональной структурах. Если вся структура соединения построена из таких единиц, ее можно рассматривать или как структуру металла с занятыми междоузлиями, или как структуру, построенную главным образом из координационных полиэдров. [16]
Кристаллическая структура шпинелевидных соединений кобальта - кубическая, длина ребра элементарного куба составляет 8 09 А для алюмината и станната кобальта и 8 3 А - для хромита. [17]
 |
Изображение структуры Y. [18] |
Кристаллическая структура соединения типа Y - 2BaO - 2MeO - 6Fe203 изображена на рис. 1.17. В гексагональную элементарную ячейку входит 18 слоев ионов 02 -; с т 4 356 нм. Структура соединения может быть построена из шпинельных блоков S и Т, структура которых показана на рис. 1.16, а. В блоках Т катионы занимают тет-ра - и октаэдрические пустоты, причем на т один блок приходится два иона с тетраэдрической координацией и шесть - с октаэд-рической. Ионы кислорода и бария образуют плотную упаковку гексагонального типа, поэтому чередование блоков S и Т также приводит к гексагональному типу всей решетки. [19]
Типы кристаллических структур соединений ABCU весьма разнообразны. Многие оксиды АВС4 имеют полиморфные модификации при атмосферном давлении и претерпевают структурные превращения при повышении давления. Диапазон структурных различий этих соединений очень широк; от структур типа кварца с тетраэдрическим окружением атомов А и В до оксосолей, содержащих обособленные ионы ВС4 и атомы А с высокими координационными числами. Некоторые из этих структур приведены в табл. 13.8; отметим здесь только некоторые общие моменты. [20]
Деталей кристаллической структуры соединения СезОа в работе [2] не приведено. В работе [3] подтверждено, что решетка фазы CeGaa гексагональная, однако с большим отношением периодов, чем было установлено ранее: а 4 32 А, с 4 34 А. [21]
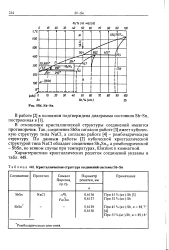 |
Кристаллическая структура соединений системы Sb-Sn. [22] |
В отношении кристаллической структуры соединений имеются противоречия. Так, соединение SbSn согласно работе [3] имеет кубическую структуру типа NaCl, а согласно работе [4] - ромбоэдрическую структуру. По данным работы [2] кубической кристаллической структурой типа NaCl обладает соединение Sb2Sn3, а ромбоэдрической - SbSn, во всяком случае при температурах, близких к комнатной. [23]
Сведения о кристаллической структуре соединений приведен. [24]
Сведения о кристаллической структуре соединений Pu5Sn3, Pu5Sn4, PugSn7, Pu7Sn8 отсутствуют. [25]
Сведения о кристаллических структурах соединений, обнару -: енных и расшифрованных различными исследователями, противо-ечивы. [26]
Нами детально исследована кристаллическая структура соединения с элементарной ячейкой, составленной из четырех подъячеек. [27]
Одновременно происходит разрушение кристаллической структуры соединения. Вероятно, вода в этих комплексах является составной частью их кристаллической решетки. Обезвоженное соединение KHfOF3 при 350 - 450 С переходит в кристаллическое состояние, что сопровождается увеличением числа линий на дифрактограмме и появлением двух экзотермических эффектов на кривой нагревания. При температуре 450 С происходит частичная потеря фтора ( в виде 0 3 молей HF) и удаление следов воды. Прокаленный KHfOF3 нерастворим в воде, соляной и азотной кислотах; растворяется в плавиковой кислоте, а также в концентрированных серной и азотной при нагревании. [28]
Когда необходимо исследовать кристаллическую структуру соединения, которое при комнатной температуре находится в газообразном или жидком состоянии. [29]
 |
Кристаллическая структура соединений системы S-Yb. [30] |
Страницы: 1 2 3 4 5