Тетрагональная структура
Cтраница 1
Тетрагональная структура Ni3P подтверждена в работе [2], где получены значения а 8 954 А, с 4 387 А. [1]
 |
Магнитные свойства соединений урана со структурой типа ThsP4. [2] |
Тетрагональная структура этого типа характерна для соединений урана состава UX2, где X - Р, As, Sb, Bi. [3]
Тетрагональная структура, образует минерал куперит, пр. Устойчив на воздухе, при прокаливании образует Pt. Уже при комнатной температуре в атмосфере водорода происходит восстановление до Pt и H2S, сопровождающееся раскаливанием. Не растворяется в кислотах, царской водке и щелочах. [4]
 |
Магнитные свойства соединений урана со структурой типа Th3P4. [5] |
Тетрагональная структура этого типа характерна для соединений урана состава UX2, где X - Р, As, Sb, Bi. [6]
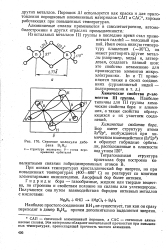 |
Строение молекулы дибо-рана В2Нв. [7] |
Тетрагональная структура кристалла бора построена ко-валентными связями гибридизированных атомов В. [8]
 |
Строение молекулы дибо-рана В2Н6. [9] |
Тетрагональная структура кристалла бора построена ковалентными связями гиб-ридизированных атомов В. [10]
Тетрагональная структура кристалла бора построена ковалентными связями гибридизи-рованных атомов В. [11]
Имеет тетрагональную структуру с параметрами решетки: а3 925 А и с3 238 А; плотн. [12]
В тетрагональной структуре атомы имеют тетраэдрическую координацию, каждый атом цинка окружен четырьмя атомами фосфора, в то время как каждый атом фосфора - двумя атомами цинка и двумя атомами фоосфора. Четыре связи Zn - Р имеют длину 2 40 А, а две связи Р - Р - 2 19 А, что является причиной незначительного тетраэдрического деформирования. Структура тетрагональной модификации ZnP2, определенная в результате рентгенографического исследования монокристаллов [15], представлена на рис. III.2. Показаны четыре элементарные ячейки, атомы фосфора образуют спиральные цепочки. [13]
В тетрагональной структуре СиАЬ атомы Си, имеющие тетрагонально-антипризматическую координацию, соединены в цепи, параллельные оси Z; антипризмы сочленяются друг с другом квадратными гранями в колонны. [14]
Наиболее известна тетрагональная структура, с использованием которой и было получено большинство рентгеноструктурных данных. По мнению самого Филлипса [5], тетрагональная структура кристаллического лизоцима имеет один серьезный недостаток - молекулы фермента в ней подходят друг к другу особенно плотно и взаимодействуют в области участков Е и F активного центра, что не позволяет наблюдать связывание Сахаров с данными участками без разрушения кристаллов. Это, видимо, стимулировало изучение других кристаллических форм лизоцима [29-31], хотя и без особого успеха в выявлении новых деталей строения активного центра и механизма его действия. В настоящее время надежды возлагаются на лизоцимы из других источников, такие как лизоцим из белка яиц черепахи [34], четвертичная структура которого практически идентична лизоциму из белка куриных яиц, но кристаллы содержат аномально большое количество воды. Возможно, в этом случае активный центр фермента будет более доступен для аналогов субстрата и эффекторов и соответствующий рснгсноструктурный анализ приведет к более определенным выводам о топографии связывающих участков активного центра. [15]
Страницы: 1 2 3 4 5