Модельный субстрат
Cтраница 1
Модельный субстрат укладывается в глубокий разрез молекулы лизоцима и фиксируется водородными связями. [1]
Синтезированы модельные субстраты каркасного строения, включающие моно-и полизамещенные гомологи адамантана, его функциональные производные, подобные по строению каркасные субстраты. [2]
Зависимости гидролиза олнгосахаридных модельных субстратов лизоцима, с одной стороны, и бактериальной клеточной стенки, с другой, являются различными. В отличие от этого константа скорости бактериолитического действия лизоцима контролируется ионогенными группами с рК 5 0 и 9 2, первая из которых является каталитической и участвует в реакции в анионной форме. Вторая группа, как показано при изучении конфор-мационной стабильности лизоцима под действием ультразвука, в паре с противоположно заряженной ионогенной группой, имеющей аномально низкое значение рК ( ниже 2 0), может образовывать солевой мостик, поддерживая каталитически активную конформацию активного центра фермента. В кинетике ферментативного лизиса клеточной стенки проявляется только группа с рК 5 0 ( по-видимому, карбоксилат-ион Asp 52), функция которого может заключаться в стабилизации образующегося в каталитической реакции карбокатиоиа. [3]
Молекула типа ДДТ может служить модельным субстратом по крайней мере для четырех различных типов воздействия многофункциональной оксидазы: 1) кольцевого гидраксилирования; 2) О-деалкилирования; 3) сульфидного окисления; 4) окисления боковой цепи. [4]
Не исключено, что принципиальные особенности ферментативной деструкции нерастворимой бактериальной клеточной стенки и растворимых модельных субстратов различны, как, например, различен вид рН - зависимостей их гидролиза. Поэтому необходимы более широкие исследования закономерностей ферментативного гидролиза пентидогликаиов как более близких по строению к природным субстратам лизоцима. Это же относится и к другим бактерйолитическим ферментам - гликозидазам, амидазам и пептидазам. [5]
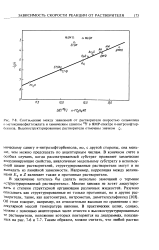
Другими словами, SbQ5 и Et3PO сильнее сольватируются в структурированных растворителях, чем все другие рассмотренные модельные субстраты. Это объясняется следующим образом. [6]
В дрожжевой синтезирующей системе наличие каждой из постулированных ферментативных активностей может быть продемонстрировано с помощью модельных субстратов. [7]
Один из возможных путей для получения ответа на поставленные вопросы, вероятно, состоит в использовании простых модельных субстратов фермента а-химотрипсина. [8]
В конечном счете в особых случаях, когда рассматриваемый субстрат проявляет химические координирующие свойства, аналогичные модельному субстрату в используемой шкале растворителей, структурированные растворители могут и не выпадать из линейной зависимости. Например, корреляция между величинами Е и Z включает также и протонные растворители. [10]
С этим трудно согласиться, поскольку истинные природные субстраты лизоцима содержат пептидные заместители, в отличие от приведенных выше модельных субстратов. Не исключено, что именно такие пептидогликаны являются наиболее специфическими субстратами и характеризуются высокими значениями кинетических параметров ферментативного гидролиза. [11]
 |
Стереоизображение молекулы карбоксипептидазы А. [12] |
Представлен вид молекулы вдоль оси В. Модельный субстрат КБЗ-А1а-А1а-Туг занимает выемку связывания субстрата и полость, примыкающую к атому цинка. Слева видны несколько больших спиральных участков. В центре молекулы находится участок с 3-структурой. Ди-сульфидная связь расположена в нижней правой части рисунка. [13]
Лизоцим - наиболее изученный представитель бактсриолнти-ческих ферментов ( 3 ], роль которых заключается в деградации бактериальной клеточной стенки. В настоящем разделе будет рассмотрено только действие лизоцима па бактериальную клеточную стенку и на некоторые модельные субстраты, так как на примере этих реакций можно продемонстрировать основные закономерности кинетики и механизмов действия, а также субстратной специфичности ферментов, осуществляющих деградацию сложных биополимеров. В качестве основного объекта рассмотрения выбран лизоцим белка куриных яиц, поскольку структура этого фермента и его активного центра уже много лет является предметом детального исследования с помощью самых разнообразных физических и физико-химических методов, и в первую очередь рентгеноструктурного анализа. [14]
Биодеградация лигнина - это окислительный процесс, осуществляемый в первую очередь грибами. Высвобождающейся при этом энергии, по-видимому, недостаточно для обеспечения роста микроорганизмов. Сегодня изучению микробиологических и биохимических аспектов деградации лигнина уделяется все больше внимания. Показано, что в эксперименте внеклеточные ферменты гриба Phanerochaete chrysosporium могут осуществлять деградацию лигниновых модельных субстратов, при этом в процессе окислительного расщепления пропильных боковых цепей лигнина участвует перекись водорода. [15]
Страницы: 1 2