Сульфат - европий
Cтраница 1
Сульфат европия ( 2) - белая мелкокристаллическая соль с удельным весом 4 98 при 25, изоморфна с сульфатом стронция и бария и только слегка растворима в воде. [1]
Кристаллический сульфат европия ( II) заметно не изменяется на воздухе в течение месяцев. [2]
Метод заключается в растворении навески образца сульфата европия, осаждении европия раствором аммиака и последующем титровании сульфат-ионов при рН 5 5 - 5 6 в среде 40 % - ного спирта в присутствии индикатора карбоксиарсеназо. [3]
Метод заключается в растворении навески образца сульфата европия, осаждении европия раствором аммиака и последующем титровании сульфат-ионов при рН 5 5 - 5 6 в среде 40 % - ного спирта в присутствии индикатора карбоксиарееназо. [4]
NaOH), постепенно прибавляют около 5 г сухого сульфата европия ( 2), приготовленного по описанному выше способу. Последний фильтруют и сушат на воздухе. [5]
Форма, в отличие от сг-формы, только слегка растворяется в разбавленной серной кислоте. Смесь, содержащую плотный белый сульфат европия ( 2), охлаждают и фильтруют. Осадок промывают разбавленной соляной кислотой, а затем несколькими миллилитрами метилового спирта, содержащего соляную кислоту. Фильтрование проводят на воздухе. [6]
Смешанный карбонат был приготовлен из сульфатов европия ( III) и стронция кипячением с содой, а восстановление проводилось водородом в кварцевой трубке при 700 - 900 С. Полученный продукт, однако, был неустойчив на воздухе-в течение 40 мин. Закись самария была получена [654] в виде гидрата Sm ( OH) 2 при взаимодействии SmCl2 с NaOH. [7]
Хорошо высушенные соли европия почти не окисляются сухим воздухом, и поэтому их удобно сохранять и использовать для синтезов. Первая методика основана на приготовлении нерастворимого сульфата европия ( 2) из соединений европия ( 3), восстановленных в редукторе Джонса. [8]
Раствор хлорида европия ( 3) медленно ( со скоростью 2 мл / мин) пропускают через редуктор, а затем последний промывают 150 мл 0 10 М раствора соляной кислоты. Сперва образуется белый осадок d - модифи-кации сульфата европия ( 2) в виде перьев или пучков. Смесь нагревают в атмосфере углекислоты до 80, при этом ct - форма превращается в более устойчивую р-форму, плотную и кристаллическую, осаждающуюся в виде компактной массы. [9]
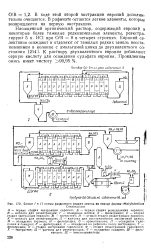 |
Блоки I а II схемы разделения редких земель на заводе фирмы Molybdenium. [10] |
К раствору двухвалентного европия добавляют серную кислоту для осаждения сульфата европия. [11]
Было бы интересно продолжить магнитные измерения европи вплоть до температуры жидкого гелия. Согласно некоторым н ( давним измерениям [ 48 б ], восприимчивость сульфата европия пр 20 К такая же, как и при 80 К. Это является хорошим подтве ждением теории. В этой статье не указывается, однако, прим ( нялся ли безводный сульфат или его гидрат, а приводятся тольк относительные восприимчивости для разных температур. [12]
Иодид европия ( II) представляет собой соединение темного коричневато-зеленого цвета, но его водный раствор почти бесцветен и медленно разлагается при комнатной температуре с выделением водорода. Фторид европия ( II) настолько энергично окисляется воздухом, что при соприкосновении с ним фильтровальная бумага загорается. Сульфат европия ( II) легко окисляется хлором, бромом, азотной кислотой и многими другими окислителями. Если карбонат европия ( II) растворять в хлорной кислоте, то получается черный перхлорат европия Eu ( ClO4) j со средней растворимостью в воде. [13]
Интересны сульфаты двухвалентных РЗЭ - самария, европия и иттербия, образующиеся при восстановлении трехвалентных РЗЭ амальгамой натрия. Эти сульфаты мало растворимы в воде, подобно сульфатам щелочноземельных металлов, с кото-рыми они изоморфны. Особенно трудно растворим сульфат европия EuSO4, растворимость которого лишь немногим больше растворимости сульфата бария. Сульфат европия бесцветен, сульфат самария ярко-красный, сульфат иттербия светло-зеленый. [14]
Пропускают ( 1250 мл) 0 1 М раствора хлорида европия со скоростью 4 мл / мин через редуктор Джонса в течение 5 часов. Процесс ведется при непрерывном токе углекислоты. Раствор с осадком а-модификации сульфата европия нагревают в атмосфере углекислоты до 80, при этом а-модификация переходит в более устойчивую плотную кристаллическую [ 3-модификацию, осаждающуюся в виде компактной массы. [15]
Страницы: 1 2