Сульфат - бериллий
Cтраница 1
Сульфат бериллия BeSO4 получается растворением окиси бериллия в горячей концентрированной серной кислоте. При 580 - 635 С BeSO4 имеет полиморфное превращение, при 760 - 830 С начинается его термическая диссоциация с выделением SO3, при 1200 - 1300 С происходит полное разложение. [1]
Сульфат бериллия хорошо растворяется в воде, его растворимость значительно увеличивается с повышением температуры. [2]
Сульфаты бериллия и магния легко растворимы, сульфаты щелочноземельных металлов растворяются с трудом, причем растворимость их сильно убывает не только при переходе от сульфата магния к сульфату кальция, но и дальше вплоть до сульфата бария. [3]
Сульфат бериллия BeSO4 образует ( подобно сульфату магния) есколько гидратов с различным количеством молекул кристаллизационной воды. Большое практическое значение имеет тот факт, что бериллий, будучи аналогом магния, а не алюминия, образует простые или двойные сульфаты, но не квасцы. Это позволяет отделять бериллий от алюминия путем кристаллизации последнего в виде алюмокалиевых квасцов, менее растворимых, чем простой или двойной сульфат бериллия-калия. [4]
Сульфат бериллия BeSO4 4Н2О - четырехводный гидрат, устойчивый на воздухе, выделяется из растворов, полученных обработкой окиси или гидроокиси бериллия разбавленной серной кислотой, после их упаривания и охлаждения. [5]
Сульфат бериллия также образует двойные соли с сульфатом аммония и с сульфатом щелочных элементов. [6]
Безводный сульфат бериллия - гигроскопичное вещество, которое получают обезвоживанием гидратированной соли при температуре около 400 С. [7]
Безводный сульфат бериллия BeS04 - бесцветные микрокристаллы с плотностью 2 443 г / сл3; разлагаются при 550 - 600 ( во влажном воздухе BeS04 переходит в BeS04 - 4H2O), плохо растворяются в конц. [8]
 |
Кривые растворимости в системах BeSO4 - ( NH4 2SO4 - Н2О ( I, MgS04 - ( NH4 2S04 - Н20 ( II. A12 ( S04 3 - ( NH4 2S04 - HaO ( III [ 8J. [9] |
Безводный сульфат бериллия получают термическим обезвоживанием четырехводного гидрата. Метод термической диссоциации сульфата используется в промышленности для получения окиси бериллия. [10]
Четырехводный сульфат бериллия не растворяется в абсолютном спирте и ацетоне. [11]
Безводный сульфат бериллия - гигроскопичное вещество, которое получают обезвоживанием гидратированной соли при температуре около 400 С. [12]
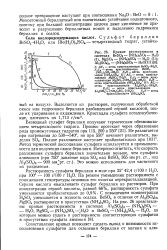 |
Кривые растворимости в системах BeSO4 - ( NH4 2SO4 - Н2О ( I, MgSO4 - ( NH4 2SO4 - Н2О ( II. A12 ( S04 3 - ( NH4 2S04 - H2O ( III. [13] |
Безводный сульфат бериллия получают термическим обезвоживанием четырехводного гидрата. Метод термической диссоциации сульфата используется в промышленности для получения окиси бериллия. [14]
Четырехводный сульфат бериллия не растворяется в абсолютном спирте и ацетоне. [15]
Страницы: 1 2 3 4