Сульфат - титан
Cтраница 1
Сульфат титана, полученный при сплавлении - окиси титана с пир осульф атом калия, растворяется в горячем 1 % - мом растворе таннина в 1 8 N серной кислоте. В этом отношении титан, как и цирконий, отличаются от тантала и ниобия. [1]
Сульфат титана ( П) Т) 8О4 известен в виде неустойчивых водных р-ров, получаемых растворением ТЮ, Т1 или Т1 ( ОН) 2 в Н28О4 при пропускании Н2; сильный восстановитель; используют при получении орг. [2]
Сульфаты титана, ниобия, тантала и церия в сернокислой среде образуют с сульфатом аммония двойные соли, в виде которых могут быть переведены в раствор; двойные соли также могут использоваться для разделения этих элементов. [3]
Сульфат титана ( 3) Ti2 ( SO4) 3 является сильным восстановителем. Характерной его особенностью является образование двойных солей типа квасцов, например Rb2SO4 - Ti2 ( SO4) 3 - 24H2O, Cs2SO4 - Ti2 ( SO4) 3 - 24H2O, по свойствам напоминающих алюминиевые квасцы. [4]
Сульфат титана ( Ш) Т12 ( 8О4) 3-зеленые кристаллы тетрагон, сингонии ( а 0 844 нм, с 2 195 нм); гшотн. С разлагается до ТЮ2; на воздухе окисляется; не раств. Из р-ров можно получить гидраты с 8 ( синие) и 5 ( фиолетовые) молекулами воды. [5]
Сульфат титана, полученный при плавлении - окиси титана с пиросульфатом калия, растворяется i горячем 1 % - иом растворе таннина в 1 8 N серной кислоте. [6]
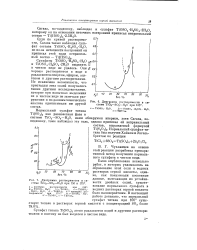 |
Диаграмма растворимости в системе ТЮ2 - S03 - Н20 при 125.| Диаграмма растворимости в системе ТЮ2 - S03 - Н20 при 150 и 175. [7] |
Сульфат титана Ti ( S04) a легко разлагается водой и другими растворителями и поэтому не был выделен в чистом виде. [8]
Бег-водный сульфат титана, Ti2 ( S04) 3, получают обработкой фиолетовых кристаллов кислого сульфата титана 3Ti2 ( S04) 3 - H2S04 - 25H20 конц. Соль представляет собой зеленый порошок, плохо растворимый в воде, спирте, эфире и легко растворимый в разб. [9]
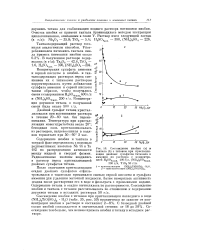 |
Соосаждение ниобия ( а и тантала ( 6 с титаном при кристаллизации двойных сульфатов титанила и аммония из раствора с концентра-цией Н2804свой 400 г / л, ( NH4 2SO4cBOO 200 г / л, ТЮ2 50 г / л. [10] |
Двойной сульфат титана кристаллизовался при выстаивании раствора в течение 20 - 60 час. [11]
Двойной сульфат титана и редкоземельных элементов в отсутствие сульфатов аммония и щелочных элементов разлагается водой с образованием сульфатов титанила и редкоземельных элементов. Сульфаты титанила при комнатной температуре хорошо растворяются в воде. Сульфаты редких земель также обладают хорошей растворимостью. При отсутствии в сплаве сульфатов аммония и щелочных металлов двойной сульфат титана и редких земель будет переходить в раствор при выщелачивании сплава водой без образования осадков; при комнатной температуре могут образоваться только кристаллогидраты сульфатов редких земель, отличающиеся крупнозернистой структурой и хорошей фильтруемостью. [12]
Двойной сульфат титана и кальция при взаимодействии с водой может давать в виде твердых фаз три сульфата: гипс, ангидрит и полугидрат. В допустимом для выщелачивания сплава температурном интервале ( 20 - 70) ангидрит всегда кристаллизуется в виде мелкозернистого осадка, который фильтруется очень плохо. Гипс и полугидрат образуют более крупные кристаллы, которые фильтруются лучше. [13]
Двойной сульфат титана и аммония в водных растворах при нагревании подвергается гидролизу с образованием гидроокиси титана. Гидролиз двойного сульфата может использоваться для получения из него двуокиси титана, в том числе титановых пигментов. [14]
Раствор сульфата титана ( III) в 4 N серной кислоте более устойчив на воздухе. [15]
Страницы: 1 2 3 4