Сульфат - редкоземельный элемент
Cтраница 1
Сульфаты редкоземельных элементов приготовляются растворением гидроокисей, карбонатов или окисей в разбавленной серной кислоте. Эти соли содержат изменяющееся количество кристаллизационной воды; их растворимость в воде уменьшается с повышением температуры. Атомные веса редкоземельных элементов были определены с помощью сульфатов. [1]
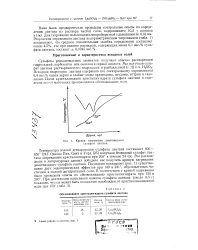 |
Кривая нагревания девятиводного сульфата лантана.| Обезвоживание кристаллогидрата сульфата лантана. [2] |
Сульфаты редкоземельных элементов получают обычно растворением гидроокисей, карбонатов или окислов в серной кислоте. [3]
Способность сульфатов редкоземельных элементов образовывать с сульфатами щелочных металлов, а также с сульфатом аммония многочисленные двойные соли известна уже давно. [4]
Полученный раствор сульфатов редкоземельных элементов ( около 3 5 л) при непрерывном перемешивании прибавляют к свежеприготовленному твердому бромату бария ( см. синтез 6), находящемуся в чашке для выпаривания. Смесь нагревают и перемешивают и, если необходимо, прибавляют еще небольшое количество бро-мата бария до полного осаждения. [5]
По этому методу раствор сульфатов редкоземельных элементов, содержащий 20 % по объему серной кислоты и 2 % сульфата аммония, кипятят с избыточным количеством висмутата натрия. По охлаждении раствор разбавляют 50 мл разбавленной ( 2: 98) серной кислоты и фильтруют через - асбест. Осадок Промывают разбавленной ( 2: 98) серной кислотой. Фильтрат обрабатывают титрованным раствором сульфата железа ( II), избыток которого титруют перманганатом. [6]
По этому методу раствор сульфатов редкоземельных элементов, содержащий 20 % по объему серной кислоты и 2 % сульфата аммония, кипятят с избыточным количеством висмутата натрия. По охлаждении раствор разбавляют 50 мл разбавленной ( 2: 98) серной кислоты и фильтруют через асбест. Осадок промывают разбавленной ( 2: 98) серной кислотой. Фильтрат обрабатывают титрованным раствором сульфата железа ( II), избыток которого титруют перманганатом. [7]
Уменьшение растворимости этой соли с повышением температуры характерно для всех кристаллогидратов сульфатов редкоземельных элементов, независимо от количества содержащейся в них кристаллизационной воды. [8]
Раскислением окиси ( гидроокиси) редкоземельного металла в серной кислоте или обработкой растворов хлорида или нитрата их сульфатом щелочного металла получают сульфаты лантаноидов, имеющие различную растворимость в воде. Сульфаты редкоземельных элементов с избытком сульфата щелочного металла образуют двойные сульфаты, различающиеся по растворимости в насыщенном растворе последнего. Осадок двойных сульфатов, полученный из растворов с концентрацией редкоземельных элементов не более 15 %, представляет собой кристаллическое вещество, легко фильтрующееся и промывающееся. Образование сульфатов и двойных сульфатов используют в технологии разделения редкоземельных элементов. [9]
Монацнтовые и бастнезитовые руды обычно вскрывают нагреванием с серной кислотой. При этом образуются сульфаты редкоземельных элементов, которые выщелачиваются из продукта реакции водой. Если редкоземельные элементы извлекают из монацитовых руд, то прежде всего стремятся выделить торий. Существует несколько способов его выделения, самым распространенным из которых является осаждение пирофосфата тория из сернокислых растворов. Редкоземельные элементы извлекают из раствора осаждением в виде оксалатов или двойных сульфатов редкоземельных элементов и натрия, а уже затем эти соединения превращают в нужную техническую соль. [10]
Химические исследования, проведенные некоторыми учеными, подтвердили лишний раз существование пробела между неодимом и самарием. Так, еще в 1914 г. Кац и Джемс исследовали гидролиз сульфатов редкоземельных элементов и пришли к выводу, что плавная кривая на графике имеет разрыв на участке неодим - самарий. [11]
Легче всего разлагаются гидроокиси и оксалаты - при 500 - 600 С. Нитраты, хлориды, сульфаты при нагревании на воздухе сначала теряют кристаллизационную воду ( - 500 - 600 С), потом образуют основные соли и лишь при более высокой температуре - окислы. Сульфаты редкоземельных элементов, например, лишь при 1000 С переходят в окислы, причем термическая устойчивость сульфатов и нитратов несколько уменьшается в ряду Се - Lu. При разложении карбонатов также сначала образуются основные соли, а потом окислы. Устойчивость карбонатов в ряду Sc - La увеличивается. [12]
Сульфаты Сег-группы выпадают в осадок, а Yttr-группы остаются в растворе. Определение электропроводности таких растворов показало, что здесь образуются комплексные сеединения. При пропускании тока через раствор сульфатов редкоземельных элементов значительная часть металла направляется к аноду. [13]
После повторного выпаривания до появления паров серной кислоты раствор разбавляют до 25 мл и оставляют стоять в течение 4 час. Фильтрат и промывные воды упаривают и удаляют всю серную кислоту нагреванием не выше 450, чтобы избежать образования окиси тория. Осадок состоит из сульфата тория с большей или меньшей примесью сульфатов редкоземельных элементов. Если применяемый колориметрический метод определения тория допускает присутствие небольшого количества редкоземельных элементов, то разделение можно закончить на этой стадии. [14]
Применяется для разложения фосфатов и некоторых нио батов. В нагретую примерно до 200 концентрированную кислоту всыпают небольшими порциями измельченный минерал и нагревают при перемешивании в течение 30 мин. Затем материал переносят в большое количество ледяной воды, ввиду того, что растворимость сульфатов редкоземельных элементов повышается с понижением температуры. Возможен также вариант с упариванием массы досуха до прекращения выделения белых паров; однако обычно он оказывается более трудоемким, несмотря на лучшее обезвоживание кремнекислоты и, следовательно, более легкое дальнейшее фильтрование. Нерастворившиеся частицы минерала либо повторно обрабатывают H2S04, либо сплавляют с бисульфатом. [15]
Страницы: 1 2