Сульфид - металл
Cтраница 2
Сульфиды металлов менее тугоплавки и менее прочны, чем их кислородные аналоги; на этом основано смазочное действие присадок, содержащих серу, при обработке сталей. Для резания низкоплавких металлов, таких, как Al, Cd, Zn и др., сульфиды которых плавятся при значительно более высокой температуре, применение СОЖ, содержащих серу, нецелесообразно. Для резания этих металлов часто рекомендуются СОЖ на основе жиров, мыл, органических кислот и других относительно малоактивных компонентов. [16]
Сульфиды металлов, как правило, тугоплавки и мало летучи. Расплавленные сульфиды активных металлов ( например, щелочных) электропроводны. Немногочисленные сульфиды неметаллических элементов более легкоплавки, а некоторые из них ( например, сульфид углерода CS2) сильно летучи, в жидком состоянии электричества не проводят и кристаллизуются в решетках молекулярного типа. [17]
Сульфиды металлов обладают различной тер-мич. Bi, Sb, As, Cu, Ag диссоциируют при нагревании до 1 000, CdS - ок. Галоиды окисляют сульфиды с образованием солей металлов и галоидных производных серы. Галоидов о дор оды энергично реагируют с образованием С. Кислород при обыкновенной t не окисляет сухих сульфидов металлов; в присутствии влаги или в водной среде этот процесс идет с заметной скоростью. При нагревании на воздухе сульфиды окисляются до сульфатов. Если сульфаты обладают большой упругостью термич. Очень часто образующийся сульфат восстанавливается сульфидом, что усложняет ход реакции. С водой при t выше 300 - 400 сульфиды, нерастворимые в воде, но растворимые в к-тах, реагируют с образованием С. Нерастворимые в к-тах сульфиды реагируют с водяным паром лишь при белом калении, восстанавливаясь до металла. Углерод при высоких t восстанавливает сульфиды Cu, Sb, Pb, Bi до металлов; сульфиды щелочных и щелочноземельных металлов и группы железа образуют карбиды; сульфиды Мп и А1 не реагируют с углеродом. [18]
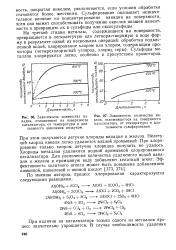 |
Зависимость количества ва.| Зависимость количества никеля, отложившегося на поверхности катализатора, от температуры и длительности сульфирования. [19] |
Сульфиды металлов хлорируются легко, особенно в присутствии промоторов. [20]
Сульфиды металлов имеют кристаллическую структуру, тугоплавки, многие характерно окрашены. [21]
Сульфиды металлов обладают различной термич. Bi, Sb, As, Cu, Ag диссоциируют при нагревании до 1 000, CdS-ок. Галоиды окисляют сульфиды с образованием солей металлов и галоидных производных серы. Галоидоводороды энергично реагируют с образованием С. Кислород при обыкновенной t не окисляет сухих сульфидов металлов; в присутствии влаги или в водной среде этот процесс идет с заметной скоростью. При нагревании на воздухе сульфиды окисляются до зульфатов. Если сульфаты обладают большой упругостью термич. Очень часто образующийся сульфат восстанавливается сульфидом, что усложняет ход реакции. С водой при t выше 300 - 400 сульфиды, нерастворимые в воде, но растворимые з к-тах, реагируют с образованием С. Нерастворимые в к-тах сульфиды реагируют с зодяным паром лишь при белом калении, вос -: танавливаясь до металла. Углерод при высо-ix t восстанавливает сульфиды Cu, Sb, Pb, Bi до металлов; сульфиды щелочных и щелочно-юмельных металлов и группы железа образует карбиды; сульфиды Мп и А1 не реагируют с углеродом. [22]
Сульфиды металлов охватывают обширную группу нормальных сульфидов, в молекулах которых между собой не связаны ни атомы серы, ни атомы металлических элементов, и сравнительно незначительные группы субсульфидов, в которых атомы металлических элементов связаны друг с другом, и тиосульфидов, или персульфидов, в которых связаны друг с другом атомы серы. В тиосульфидах содержатся группировки из двух или большего числа атомов серы с отрицательным окислительным числом, почему их иногда называют полисульфидами. [23]
Сульфиды металлов называются блесками, или колчеданами. [24]
Сульфиды металлов ускоряют главным образом реакции дегидрирования боковой цепи алкилтиофена и его разложения с выделением сероводорода. Кинетические исследования показывают, что эти реакции протекают независимо и подчиняются уравнению первого порядка. [25]
 |
Гидрирование сульфолена-2 в присутствии сульфидов металлов. [26] |
Сульфиды металлов проявляют активность при высокой температуре [380], поэтому их можно использовать лишь для восстановления термически стойких непредельных сульфонов. [27]
Сульфиды металлов способствуют пластическому течению выступов на поверхности прирабатываемых деталей, благодаря чему ускоряется сглаживание шероховатых поверхностей и уменьшается удельная нагрузка на фактической площади контакта трущихся деталей. [28]
Сульфиды металлов этой группы, особенно щелочных и щелочноземельных, образуются из элементов с выделением большого количества тепла, причем количество тепла на атом серы уменьшается с увеличением относительного содержания серы в сульфидах; наряду с этим уменьшаются также термическая и химическая стойкость. [29]
Сульфиды металлов ( As, Sb, Ge, Sn и некоторых других) растворяются в растворах сульфидов щелочных металлов и аммония с образованием тиосолей. [30]
Страницы: 1 2 3 4