Сульфид - щелочноземельный металл
Cтраница 3
Поэтому их растворы имеют сильно щелочную реакцию. Нейтральные сульфиды щелочноземельных металлов как таковые в воде не растворяются. Однако при действии воды они претерпевают гидролитическое расщепление 2CaS 2HOH Ca ( HS) 2 - f - Ca ( OH) 2, а образующийся при этом кислый сульфид переходит в раствор. Кислоты разлагают все эти сульфиды с выделением сероводорода. [31]
В сульфидах, селенидах, теллуридах и арсенидах имеются различные виды химической связи - от ионных до ковалентных и металлических. Например, сульфиды щелочноземельных металлов имеют решетки ионной связи; пирит FeS2, арсенопирит ( FeAs) S и другие характеризуются ковалентными связями; в кристалле ковеллина Cu3S S2 имеются два типа атомов серы: группы S2 между шестью атомами меяи и изолированные атомы серы, окруженные пятью атомами меди. [32]
Моносульфиды представлены во всех-введенных выше группах а, б и в. MgS и сульфиды щелочноземельных металлов образуют ионные кристаллы, однако1 тот же тип структуры ( NaCl) реализуется и в случае MnS ( но больше ни у каких других моносульфидов З - элементов), а также у соединений 4f - и 5 / - элементов. Это свидетельствует о том, что геометрическое сходство структур не означает сходства в характере связей; подтверждением тому - серебристо окрашенный PbS и металлический золотистый цвет LaS. Моносульфиды переходных металлов ( группа б) рассматриваются; немного позднее. [33]
Сульфид цинка применяют в качестве основания при изготов-линии светосоставов как временного, так и постоянного действия. Для светосоставов временного действия используют также сульфиды щелочноземельных металлов. [34]
Области применения сульфидов весьма широки. Многие сульфиды, особенно сульфиды переходных металлов, лантаноидов и актиноидов, обладают ценными магнитными, термоэлектрическими, каталитическими и другими свойствами. Сульфиды щелочноземельных металлов CaS, SrS, BaS применяют как основу многих люминофоров. MgS тугоплавок и перспективен для огнеупоров, у CdS сильно выражены фотоэлектрические свойства. [35]
Люминофоры на основе сульфидов щелочноземельных металлов имеют глубокие электронные ловушки, что позволяет получать наиболее длительное послесвечение. В качестве активаторов в этих люминофорах используют тяжелые металлы Bi, Си, РЬ, Ми, а также редкоземельные элементы. Основной недостаток люминофоров на основе сульфидов щелочноземельных металлов - их гидролитическое разложение влагой воздуха, при котором теряются их люминесцентные свойства. [36]
Существенное значение имеет то, чтобы тигель был плотно закрыт. В частности, таким способом получают люминофоры на основе сульфидов щелочноземельных металлов. [37]
Попытки использовать люминесцентные свойства некоторых пигментов для приготовления светящихся печатных красок предприншмались уже довольно давно. Задача не очень сложна, когда речь идет о получении оттисков, предварительно подвергаемых действию естественных или искусственных источников люминесценции и частично излучающих свет в течение ограниченного времени. Применяемые для этой цели фосфоресцирующие пигменты получают на основе сульфидов цинка, содержащих чуть заметные следы ( меньше 0 001 %) примесей, или на основе сульфидов щелочноземельных металлов с небольшой примесью висмута, меди или редкоземельных металлов в присутствии специальных флюсов, из которых лучшими являются, по-видимому, соли лития. Для сохранения активности эти пигменты не должны быть очень тонко измельчены, а это ограничивает возможность применения красок, которые их содержат. [38]
Он нашел не известный ему ранее минерал ( тяжелый пшат) и прокалил его с углем, после чего обнаружил, что получившийся препарат светится в темноте. Препараты, пригодные для использования 6 качестве светящихся красок, технически впервые получил в 70 - х гг. прошлого столетия англичанин Балмейн ( Balmain), после того как было установлено, что свойство прокаленных сульфидов щелочноземельных металлов светиться зависит от присутствия в них следов солей тяжелых металлов. По мнению Ленарда ( Lenard), получение фосфора определяется тремя компонентами: 1) сульфидом, 2) флюсом, 3) тяжелым металлом. [39]
Он нашел не известный ему ранее минерал ( тяжелый шпат) и прокалил его с углем, после чего обнаружил, что получившийся препарат светится в темноте. Препараты, пригодные для использования в качестве светящихся красок, технически впервые получил в 70 - х гг. прошлого столетия англичанин Балмейн ( Balmain), после того как было установлено, что свойство прокаленных сульфидов щелочноземельных металлов светиться зависит от присутствия в них следов солей тяжелых металлов. По мнению Ленарда ( Lenard), получение фосфора определяется тремя компонентами: 1) сульфидом, 2) флюсом, 3) тяжелым металлом. [40]
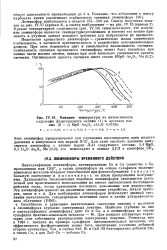 |
Влияние температуры на интенсивность излучения фторгерманата магния ( 1 и арсената магния ( 6 - х MgO - As2O5 - iLi20 - 0 01Mn. [41] |
Способность к запасанию значительных светосумм связана с наличием в люминофорах глубоких электронных ловушек. Наиболее глубокие из них в цинксульфидных люминофорах дают Си и Со, а в люминофорах на основе сульфидов щелочно-земельных металлов - Bi. Для каждого активатора характерно свое собственное распределение электронных ловушек. Ротшильд еще в 1963 г. показал на примере сульфидов щелочноземельных металлов, что эффективность фосфоресценции может быть значительно улучшена добавкой второго активатора. [42]
Природные сульфиды составляют основу руд цветных и редких металлов и широко используются в металлургии. Некоторые из них служат также сырьем для получения серной кислоты. Сульфиды щелочных и щелочноземельных металлов находят применение в химической и в легкой промышленности. Так N328, CaS и BaS применяются в кожевенном производстве для удаления волосяного покрова с кож. Сульфиды щелочноземельных металлов, цинка и кадмия служат основой люминофоров ( см. стр. Некоторые сульфиды обладают полупроводниковыми свойствами и применяются в электронной технике. [43]
Природные сульфиды составляют основу руд цветных и редких металлов и широко используются в металлургии. Некоторые из них служат также сырьем для получения серкой кислоты. Сульфиды щелочных и щелочноземельных металлов находят применение в химической и в легкой промышленности. Так Na2S, CaS и BaS применяются в кожевенном производстве для удаления волосяного покрова с кож. Сульфиды щелочноземельных металлов, цинка и кадмия служат основой люминофоров ( см. стр. Некоторые сульфиды обладают полупроводниковыми свойствами и применяются в электронной технике. [44]
Природные сульфиды составляют основу руд цветных и редких металлов и широко используются в металлургии. Некоторые из них служат также сырьем для получения серной кислоты. Сульфиды щелочных и щелочноземельных металлов находят применение в химической и в легкой промышленности. Так Na2S, CaS и BaS применяются в кожевенном производстве для удаления волосяного покрова с кож. Сульфиды щелочноземельных металлов, цинка и кадмия служат основой люминофоров ( см. стр. Некоторые сульфиды обладают полупроводниковыми свойствами и применяются в элек-тронной технике. [45]
Страницы: 1 2 3 4