Сульфид - тип
Cтраница 2
Вот почему сульфиды типа KtS ( например, MnS, FeS и другие), для которых TIPKts10 - 27, осаждают сероводородом в щелочной среде, а осаждение катионов IV аналитической группы ведут в кислой среде. [16]
Вот почему сульфиды типа KtS, для которых FlPicts 10 - 27, осаждают сероводородом в щелочной среде, а осаждение сульфидов катионов IV аналитической группы ведут в кислой среде. [17]
Вот почему сульфиды типа KtS, для которых ПРК ( 810 - 27, осаждают сероводородом в щелочкой среде, а ссаждсние сульфидов катионов IV аналитической группы ведут в кислой среде. [18]
Вот почему сульфиды типа KtS ( например, MnS, FeS и другие), для которых ПРК13 10 - 27, осаждают сероводородом в щелочной среде, а осаждение катионов IV аналитической группы ведут в кислой среде. [19]
Распад при ЭУ сульфидов типа в которых атом серы удален от ароматического ядра, более сложен. Однако здесь всегда можно идентифицировать процессы, обусловленные р-разрывами и разрывами связей С - S по обе стороны от атома серы. Для таких соединений значительную долю полного ионного тока составляют фрагменты, включающие ароматическое кольцо. [20]
Из сульфидов легче всего обессериваются сульфиды бензильного типа, за ними следуют алкиларил - и диалкилсульфиды, а наиболее устойчивы диарилсульфиды. [21]
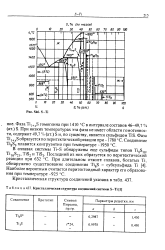 |
Кристаллическая структура соединений системы S-Ti [ 1J. [22] |
В сплавах системы Ti-S обнаружены еще сульфиды типов Ti8S) 0, Ti16S2i, TiS. Последний из них образуется по перитектической реакции при 632 С. Наиболее вероятным считается перитектоидный характер его образования при температуре - 925 С. [23]
Элементы подгруппы мышьяка с серой образуют сульфиды типа Э253 и Э255, сходные, в химическом отношении с окислами этих элементов. Изучение химических свойств As, Sb и Bi и их соединений показывает, что они, особенно мышьяк, сходны с фосфором. [24]
Из уравнения ( 7) видно, что растворимость сульфида типа возрастает прямо пропорционально квадрату концентрации ионов водорода. [25]
Из уравнения ( 7) видно, что растворимость сульфида типа KtS возрастает прямо пропорционально квадрату концентрации ионов водорода. [26]
Из уравнения ( 7) видно, что растворимость сульфида типа KtS возрастает прямо пропорционально квадрату концентрации иондв водорода. [27]
Из уравнения ( 7) видно, что растворимость сульфидов типа KtS возрастает прямо пропорционально квадрату концентрации ионов водорода. [28]
Из уравнения ( 7) видно, что растворимость сульфида типа KtS возрастает прямо пропорционально квадрату концентрации ионов водорода. [29]
В ряде работ [8, 11, 12, 37, 51-54] приводятся колебательные спектры или таблицы частот сульфидов типа RSR, где R - ароматическое кольцо. [30]
Страницы: 1 2 3 4