Сульфид - фосфор
Cтраница 1
Сульфид фосфора в соотношении 1: 1 с сульфидом мышьяка дает стекло только при режиме охлаждения 2ПО - 300 С в секунду. При более медленном охлаждении сплав получается кристаллическим. [1]
Сульфид фосфора ( V) для фосфоросернения дозируют, в аппарат 27 в количестве 21 % ( в расчете на алкилфенол) в виде суспензии в смеси с маслом-разбавителем. Поскольку реакция фосфоросернения является экзотермической, суспензию сульфида фосфора ( V) подают равномерно в течение 2 ч при 85 С. Для предупреждения вспенивания в смесь добавляют 0 005 % противопенной присадки ПМС-200А; реакторы для фосфоросернения оснащены пеногасителями. Выделяющийся при фосфоро-сернении сероводород поступает в абсорбер 36, где нейтрализуется 20 % - ным раствором едкого натра. Чтобы облегчить отделение сероводорода от фосфоросерненного продукта, а также для создания безопасных условий процесса через продукт барботируют азот. Процесс нейтрализации осуществляют в аппарате 31 путем смешения продукта фосфоросернения с осушенной суспензией гидроксида бария - в масле М-11. Высушенный продукт освобождают от механических примесей путем фильтрования на рамных фильтр-прессах через бель-тинг и фильтровальную бумагу при 150 - 160 С или на центрифугах ОПН-1005у при 100 - 110 С. [2]
Сульфид фосфора ( V) P2Ss подобно P2Os существует в виде нескольких модификаций. [3]
Сульфиды фосфора получают при сплавлении фосфора с серой в атмосфере двуокиси углерода. Для этой цели используют красный, фосфор ( так как белый реагирует слишком энергично) или же медленно испаряют сероуглерод из раствора, содержащего фосфор и серу. Все эти соединения можно щерекристаллизовать из соответствующих растворителей или же переплавить; в чистом виде они дают хорошо образованные желтые кристаллы. [4]
Сульфиды фосфора получают при сплавлении фосфора с серой в атмосфере двуокиси углерода. Для этой цели используют красный фосфор ( так как белый реагирует слишком энергично) или же медленно испаряют сероуглерод из раствора, содержащего фосфор и серу. Все эти соединения можно перекристаллизовать из соответствующих растворителей или же переплавить; в чистом виде они дают хорошо рбразованные желтые кристаллы. [5]
Сульфид фосфора ( V) очищают возгонкой в трехколенной стеклянной трубке в слабом токе сухого оксида углерода ( IV) при 500 - 550 С или перекристаллизацией из горячего сероуглерода, в котором он немного растворяется. На влажном воздухе вещество подвергается гидролизу. [6]
Сульфид фосфора облучают быстрыми нейтронами и растворяют в сероуглероде. [7]
Сульфиды фосфора P4S3, P4S7 и P4S10 получают нагреванием серы при 100 с белым фосфором или при 250 с красным фосфором. Структура так называемого сульфида фосфора Р48ю аналогична структуре окиси Р4Ою ( рис. 130, стр. Сульфиды фосфора нерастворимы в воде, но легко гидролизуются, образуя H2S и кислородные кислоты фосфора. [8]
Сульфиды фосфора получают при сплавлении фосфора с серой в атмосфере двуокиси углерода. Для этой цели используют красный фосфор ( так как белый реагирует слишком энергично) или же медленно испаряют сероуглерод из раствора, содержащего фосфор и серу. Все эти соединения можно перекристаллизовать из соответствующих растворителей или же переплавить; в чистом виде они дают хорошо образованные желтые кристаллы. [9]
Малоядовитый сульфид фосфора, применяемый иногда в производства спичек, дает все реакции желтого фосфора, но отравлений им до сих пор но наблюдалось. [10]
Другой сульфид фосфора P2S5, называемый пснтасульфидом, получают так же, как описало выше, но для реакции берут на J вес. После окончания реакции продукт переносят в трубку из тугоплавкого стекла и отгоняют при 500 - 514 С в токе СО2 около половины его количества. Возгон снимают со стенки трубки, измельчают и экстрагируют в колбе с обратным холодильником или в экстракционном аппарате горячим сероуглеродом ( па 1 вес. Затем сероуглерод отгоняют в вакууме. Выпавшие светло-желтые кристаллики сульфида быстро переносят в пробирку для яапаивания и запаивают. [11]
Все сульфиды фосфора - желтые кристаллические вещества; их молекулярные массы ( определенные либо в растворе CS2, либо в парообразном состоянии) соответствуют приведенным выше формулам. Все эти фазы получаются при прямом взаимодействии элементов в различных условиях. Между ними прослеживаются интересные взаимосвязи. Хотя все указанные молекулы описываются общей формулой P4Sn, они, как это следует из структурных исследований, не содержат группу Р4 в качестве общей структурной единицы. Конфигурация молекулы a - P4S4 подобна конфигурации As4S4 ( рис. 20.15, а), но если расстояние As-As в минерале реальгаре имеет обычное значение, то длины связей Р - Р очень велики. Для P4S4 выделена и вторая ( 3) модификация [ Chem. ЯМР и химического анализа, по монокристаллы этой модификации, пригодные для структурных исследований, вырастить, как выяснилось, невозможно. Полезно также ознакомиться со строением третьей кристаллической модификации - As4S4 ( разд. [12]
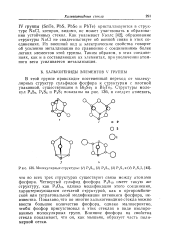 |
Молекулярные структуры. ( / P4S5, ( 2 P4S7, ( 3 P4S, и ( 4 P4S3b. [13] |
Четвертый сульфид фосфора Р45ю имеет такую же структуру, как Р & ю, однако модификация этого соединения, характеризующаяся сетчатой структурой, как в орторомбиче-ской или тетрагональной модификации пятиокиси фосфора, неизвестна. Показано, что во многие халькогенидные стекла можно ввести большое количество фосфора, однако маловероятно, чтобы фосфор присутствовал в этих стеклах в виде изолированных молекулярных групп. Влияние фосфора на свойства стекла показывает, что он, как мышьяк, образует часть полимерной сетки. [14]
Другой сульфид фосфора P2S6, называемый пентасульфидом, получают так же, как описано выше, но для реакции берут на 1 вес. После окончания реакции продукт переносят в трубку из тугоплавкого стекла и возгоняют ( при 500 - 514 в токе СО2) около половины его количества. Возгон снимают со стенки трубки, измельчают и экстрагируют в колбе с обратным холодильником или в экстракционном аппарате горячим сероуглеродом ( на 1 вес. Затем сероуглерод отгоняют в вакууме. Выпавшие светложелтые кристаллики сульфида быстро переносят в пробирку для запаивания и запаивают. [15]
Страницы: 1 2 3 4