Сульфид - цирконий
Cтраница 1
Сульфид циркония, подобно сульфидам хрома и алюминия, может быть получен только сухим путем. [1]
Серые кристаллы сульфида циркония ( ZrS2) n устойчивы в воде и в разбавленных кислотах. Наибольшей жаростойкостью обладают, однако, полимерные карбиды циркония ( ZrC) n, так же как и карбиды других элементов этой группы периодической системы - титана, гафния и тантала. [2]
 |
Сверхструктуры нестехиометрических окислов и халькогенидов со структурой В1 ( типа NaCl. [3] |
Аналогичная картина наблюдается и для окиси ниобия, сульфида циркония и селенида и сульфида иттрия. Такую структуру образуют некоторые сульфиды и другие соединения переходных металлов и рутения. В этих соединениях сосуществуют тетраэдрическая и октаэдрическая координации и отсутствует широкий интервал составов. [4]
В некоторых работах [ 48, 691 указано, что сульфиды циркония, по-видимому, реагируют с кальцием с образованием металла, однако сообщении о проведении подобных экспериментов не имеется. [5]
Последние работы позволили в значительной мере выяснить вопросы, связанные с существованием сульфидов циркония. Предполагают, что удвоенное значение периода с, полученное в работе [2], связано с двой-никованием использованных монокристаллов. [6]
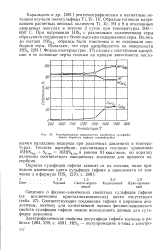 |
Температурная зависимость продуктов сульфиди-зации двуокиси гафния сероводородом. [7] |
Соответствующие соединения гафния и циркония аналогичны, поэтому для качественной оценки физико-химических свойств сульфидов гафния можно использовать данные для сульфидов циркония. [8]
Какие из перечисленных ниже соединений могут иметь достаточно широкую область гомогенности: окислы вольфрама, окись магния, двуокись кремния, сульфид циркония, нитрид циркония, закись меди, трехокись сурьмы. [9]
ZrS не взаимодействуют с разбавленной H2SO4 и щелочами. В отличие от них ZrS2 медленно растворяется в разбавленной H2SO4, при нагревании гидро-лизуется в растворе NaOH. При нагревании сульфидов циркония в среде водорода и азота в присутствии углерода наблюдается ярко выраженные десульфурация и науглероживание. При 2800 С образуется карбид циркония, а при 2000 С в среде азота смесь нитрида и карбида циркония. [10]
Мелкие кусочки металла ( из проволоки) и серы помещали в тигель со специальной обмазкой. По второму методу при получении сульфида циркония использовали ZrCl4, который синтезировали из металлического циркония и че-тыреххлористого углерода; полученный ZrS2 не содержал примеси свободной серы и хлора. Дисульфид циркония может быть также получен при действии сероводорода на двуокись циркония при 1500 С. [11]
В работе [59] показано, что некоторые смешанные окислы висмута и других металлов [ Zr, Th, Sn ( IV) ] имеют в нейтральных растворах высокую селективность по от -, ношению к ионам хлора. Продукт, представляющий собой фосфоросурьмяную кислоту [95], полученный добавлением пятихлористой сурьмы к фосфорной кислоте и высушенный при 80, показал обратимую сорбцию некоторых одно - и двухвалентных катионов. Хорошо сорбировавшийся калий легко вымывался 1 М растворами солей аммония. HSb ( OH) 6 - Несколько интересных ионообменников на основе циркония получено советскими исследователями [60], однако устойчивость полученных соединений довольно ограниченна. Оксалат и карбонат циркония обладают слабокислыми свойствами, подобно карбоксилатным смолам. Первый позволяет эффективно разделять лантан и кальций, второй - кальций и магний. Сульфид циркония, полученный при осаждении избытком сульфида натрия, имеет высокую селективность по отношению к ионам, образующим нерастворимые сульфиды. Это слабокислый ионообменник, емкость водородной формы которого очень мала по сравнению с емкостями других катион-ных форм. С помощью сульфида циркония было достигнуто высокое обогащение меди относительно кальция и железа. [12]
В работе [59] показано, что некоторые смешанные окислы висмута и других металлов [ Zr, Th, Sn ( IV) ] имеют в нейтральных растворах высокую селективность по отношению к ионам хлора. Продукт, представляющий собой фосфоросурьмяную кислоту [95], полученный добавлением пятихлористой сурьмы к фосфорной кислоте и высушенный при 80, показал обратимую сорбцию некоторых одно - и двухвалентных катионов. Хорошо сорбировавшийся калий легко вымывался 1 М растворами солей аммония. Несколько интересных ионообменников на основе циркония получено советскими исследователями [60], однако устойчивость полученных соединений довольно ограниченна. Оксалат и карбонат циркония обладают слабокислыми свойствами, подобно карбоксилатным смолам. Первый позволяет эффективно разделять лантан и кальций, второй - кальций и магний. Сульфид циркония, полученный при осаждении избытком сульфида натрия, имеет высокую селективность по отношению к ионам, образующим нерастворимые сульфиды. Это слабокислый ионообменник, емкость водородной формы которого очень мала по сравнению с емкостями других катион-ных форм. С помощью сульфида циркония было достигнуто высокое обогащение меди относительно кальция и железа. [13]
В работе [59] показано, что некоторые смешанные окислы висмута и других металлов [ Zr, Th, Sn ( IV) ] имеют в нейтральных растворах высокую селективность по от -, ношению к ионам хлора. Продукт, представляющий собой фосфоросурьмяную кислоту [95], полученный добавлением пятихлористой сурьмы к фосфорной кислоте и высушенный при 80, показал обратимую сорбцию некоторых одно - и двухвалентных катионов. Хорошо сорбировавшийся калий легко вымывался 1 М растворами солей аммония. HSb ( OH) 6 - Несколько интересных ионообменников на основе циркония получено советскими исследователями [60], однако устойчивость полученных соединений довольно ограниченна. Оксалат и карбонат циркония обладают слабокислыми свойствами, подобно карбоксилатным смолам. Первый позволяет эффективно разделять лантан и кальций, второй - кальций и магний. Сульфид циркония, полученный при осаждении избытком сульфида натрия, имеет высокую селективность по отношению к ионам, образующим нерастворимые сульфиды. Это слабокислый ионообменник, емкость водородной формы которого очень мала по сравнению с емкостями других катион-ных форм. С помощью сульфида циркония было достигнуто высокое обогащение меди относительно кальция и железа. [14]
В работе [59] показано, что некоторые смешанные окислы висмута и других металлов [ Zr, Th, Sn ( IV) ] имеют в нейтральных растворах высокую селективность по отношению к ионам хлора. Продукт, представляющий собой фосфоросурьмяную кислоту [95], полученный добавлением пятихлористой сурьмы к фосфорной кислоте и высушенный при 80, показал обратимую сорбцию некоторых одно - и двухвалентных катионов. Хорошо сорбировавшийся калий легко вымывался 1 М растворами солей аммония. Несколько интересных ионообменников на основе циркония получено советскими исследователями [60], однако устойчивость полученных соединений довольно ограниченна. Оксалат и карбонат циркония обладают слабокислыми свойствами, подобно карбоксилатным смолам. Первый позволяет эффективно разделять лантан и кальций, второй - кальций и магний. Сульфид циркония, полученный при осаждении избытком сульфида натрия, имеет высокую селективность по отношению к ионам, образующим нерастворимые сульфиды. Это слабокислый ионообменник, емкость водородной формы которого очень мала по сравнению с емкостями других катион-ных форм. С помощью сульфида циркония было достигнуто высокое обогащение меди относительно кальция и железа. [15]
Страницы: 1