Сульфид - германий
Cтраница 1
Сульфид германия, легко образующийся из оксида германия в присутствии водорода и сероводорода, возгоняется при температурах выше 450 С. [1]
Сульфид германия, полученный осаждением сероводородом ( см. стр. Раствор собирают во взвешенную платиновую чашку или большой тигель. На растворение осадка-расходуется незначительное количество аммиака, так как сульфид германия хорошо в нем растворим. Иногда может остаться нерастворенным небольшое количество серы, выделившейся совместно с сульфидом германия. Раствор фильтруют и промывают фильтр небольшими порциями воды до обесцвечивания промывной жидкости. К раствору прибавляют 20 мл 3 % - ной перекиси водорода и дают пройти окислению на холоду. [2]
Сульфид германия растворяют в аммиаке, взято в небольшом избытке, с добавлением перекиси водорода, свободной от фосфорной кислоты. [3]
Сульфид германия ( П) GeS получается при умеренном нагревании сульфида германия V) GeS2 в токе водорода; GeS кристаллизуется в форме красивых листочков, обладающих в отраженном свете серо-черной окраской с металлическим блеском, а в проходящем свете-ярко-красной. Из солянокислого раствора хлорида германия ( П) он осаждается сероводородом в виде красно-бурого осадка, который растворим в растворе едкого кали и в противоположность сульфиду, приготовленному сухим путем, в горячей концентрированной соляной кислоте, а также в желтом сернистом аммонии. Из раствора тиогерма-ната при подкислении осаждается белый GeS2, а из раствора едкого кали - неизменившийся красно-бурый GeS. Последний имеет большую склонность к образованию коллоидных растворов. Сульфид германия ( П) кристаллизуется в ромбической системе. Он образует решетку, не наблюдавшуюся пока у других соединений: она имеет вид сильно деформированной решетки каменной соли. [4]
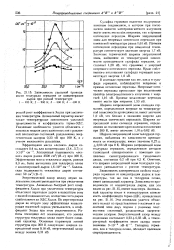 |
Зависимость удельной проводимости теллурида германия от концентрации. [5] |
Сульфид германия является полупроводниковым соединением, в котором при поглощении квантов электромагнитного излучения могут иметь место как непрямые, так и прямые оптические переходы. Значение термической ширины запрещенной зоны, найденное из температурной зависимости проводимости сульфида германия, составляет 1 58 эВ, что сравнимо с энергией непрямого оптического перехода. [6]
Сульфид германия GeS2 встречается как примесь к сульфидам цинка, меди и серебра. Источником соединений германия служит также зола некоторых сортов каменных углей. [7]
Сульфид германия очень трудно растворим и поэтому пригоден для выделения малых количеств этого элемента. [8]
Сульфид германия, полученный осаждением сероводородом ( см. стр. Раствор собирают во взвешенную платиновую чашку или большой тигель. На растворение осадка расходуется незначительное количество аммиака, так как сульфид германия хорошо в нем растворим. Иногда может остаться нерастворенным небольшое количество серы, выделившейся совместно с сульфидом германия. Раствор фильтруют и промывают фильтр небольшими порциями воды до обесцвечивания промывной жидкости. К раствору прибавляют 20 мл 3 % - ной перекиси водорода и дают пройти окислению на холоду. [9]
Сульфид германия растворяют в аммиаке, взятом в небольшом избытке, с добавлением перекиси водорода, свободной от фосфорной кислоты. Раствор кипятят до полного разложения перекиси водорода, после чего слабо подкисляют серной кислотой и разбавляют до 100 мл. В раствор вводят 20 - 25 мл 2 и. Затем осторожно при перемешивании прибавляют аммиак в таком количестве, чтобы получился избыток его в 15 - 20 мл на 100 мл раствора. Нагревают раствор до кипения, охлаждают и дают отстояться 10 - 12 час. Осадок отфильтровывают, промывают небольшими порциями разбавленного ( 1: 9) раствора аммиака, употребив его не более 50 мл, прокаливают в фарфоровом тигле так же, как пирофосфат магния ( стр. [10]
Сульфид германия ( И) GeS получается при умеренном нагревании сульфида герма-ния ( 1У) GeS2 в токе водорода; GeS кристаллизуется в форме красивых листочков, обладающих в отраженном свете серо-черной окраской с металлическим блеском, а в проходящем свете - ярко-красной. Из солянокислого раствора хлорида германия ( II) он осаждается сероводородом в виде красно-бурого осадка, который растворим в растворе едкого кали и в противоположность сульфиду, приготовленному сухим путем, в горячей концентрированной соляной кислоте, а также в желтом сернистом аммонии. [11]
Сульфид германия GeSa белый тонкий порошок, может быть получен при действии ШЗ на водный раствор окиси. Сульфид заметно растворяется в воде и легко растворяется в растворах едких или сернистых щелочей. [12]
Сульфид германия GeSj встречается как примесь к сульфидам цинка, меди и серебра. Источником соединений германия служит также зола некоторых сортов каменных углей. [13]
Сульфид германия GeS получается в виде красновато-бурого осадка при пропускании сероводорода в раствор двухлориетого германия; при повышении температуры чернеет. Плавится в инертной атмосфере при 625; при 430 начинает возгоняться; материалы, содержащие наряду с германием серу и углерод, не следует нагревать выше 400 во избежание потери германия. [14]
Сульфид германия GeS красновато-оранжевого цвета, растворим в концентрированной соляной кислоте и в растворах сульфида аммония. В концентрированных солянокислых растворах существуют анионы GeCU и др. В растворах сульфида аммония имеются сульфосоли. [15]
Страницы: 1 2 3 4