Сульфид-ионы
Cтраница 1
 |
Схема установки электрохимической очистки сточных вод от цианидов соединений. [1] |
Сульфид-ионы при рН 7 окисляются до сульфатов. При меньших значениях рН может образоваться элементная сера. [2]
Сульфид-ионы в щелочных средах образуют с нитрил о-триацетатом железа ( Ш) зеленое соединение Fe ( OH) S, окраску которого фотометрируют при 635 нм. [3]
Сульфид-ионы ускоряют анодный процесс коррозии стали. В результате действия сульфатвосстанавливающих бактерий образуется сероводород, который, соединяясь с железом, дает сернистое железо FeS. По данным некоторых исследователей, скорость коррозионного разрушения железа при воздействии этих бактерий может возрастать в 20 раз. Наиболее активными анаэробные бактерии становятся весной, что подтверждается проявлением сильной коррозии в этот период года. [4]
Сульфид-ионы должны отсутствовать, как и при определении с метиленовым синим. [5]
Сульфид-ионы вымывают 4 М водным раствором NaOH и определяют колориметрически в присутствии метиленового голубого, получаемого из 1ХГ М - тетраметил-1 4-ди-аминобензола. [6]
Сульфид-ионы можно отделить от сульфит - и тиосульфат-ионов, а также от многих других анионов осаждением их ацетатом цинка или кадмия. Тиосульфат-ионы частично увлекаются осадком. [7]
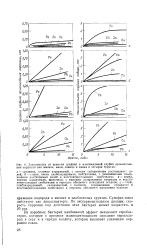 |
Зависимость от времени средней и максимальной глубин проникновения коррозии для железа, меди, свинца и цинка в четырех грунтах. [8] |
Сульфид-ионы действуют как депассиваторы. По экспериментальным данным, скорость коррозии под действием этих бактерий может возрастать в 20 раз. [9]
Сульфид-ионы окисляются до SO. К раствору, содержащему 0 1 - 0 35 ммолъ растворимого сульфида, или к суспензии малорастворимого сульфида прибавляют 20 мл 5 М раствора NaOH, 10 мл 10 % - ного раствора KI и известный объем раствора 12, перемешивают 5 мин при комнатной температуре и затем кипятят 10 мин. [10]
Сульфид-ионы, как уже было упомянуто, редко используют в качестве осадителей в весовом анализе из-за их неспецифического осаждающего действия, а также из-за неподходящих для целей весового анализа свойств. Осаждение ионов металлов в виде гидр-оксидов в большой степени страдает теми же недостатками, но все же находит применение. Примером служит осаждение Fe3 и А13 аммиаком. Метод считается наиболее точным для определения этих металлов. Использование аммиака в качестве осадителя имеет то-преимущество, что большая часть двухвалентных катионов, таких, как Cu2, Ni2, Co2, Zn2, Cd2, в аммиачной среде образует устойчивые комплексы, которые остаются в растворе. Иногда при анализе пород и минералов на определенном этапе производится осаждение соответствующих гидроксидов при помощи аммиака, их прокаливание и совместное взвешивание. Полученный результат обозначается как R2O3 и представляет собой сумму нескольких оксидов, обычно Fe2O3 А12О3 ТЮ2 PzOs, а при наличии в пробе хрома и циркония - еще и оксидов этих, элементов. При необходимости отдельные компоненты смеси оксидов можно определять раздельно. [11]
 |
Влияние концентрации NaCl на jn r,. [12] |
Сульфид-ионы участвуют в образовании продуктов коррозии железа, состоящих из гидроксида, оксида и сульфида железа ( II), которые имеют рыхлую структуру и облегчают развитие бактерий прямо на поверхности металла. [13]
Сульфид-ионы при рН 7 окисляются до сульфатов. При меньших значениях рН может образоваться элементная сера. [14]
Сульфид-ионы осаждают в виде трудно растворимых сульфидов ртути или пипка при помощи растворов сулемы или ацетата цинка и осадок отделяют. Полученный фильтрат используют для открытия SO - - ионов вышеописанным образом. [15]
Страницы: 1 2 3 4