Сумма - константа - скорость
Cтраница 3
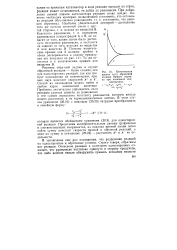 |
Кинетическая кривая Cb. ( t обратимой реакции первого порядка при начальных концентрациях. [31] |
Представив экспериментальные данные графически в соответствующих координатах, из наклона прямой линии легко найти сумму констант скорости прямой и обратной реакций, а зная их сумму и отношение (20.24) - рассчитать k и k - по отдельности. [32]
Это уравнение Михаэлиса для ферментативного катализа, где константа Михаэлиса / См представляет собой отношение суммы констант скоростей расходования промежуточного комплекса к константе скорости его образования. [33]
Выражение ( VIII-88) является уравнением реакции первого порядка, в котором константа скорости равна сумме констант скоростей обеих параллельных реакций. [34]
Что касается внутренних факторов, то их имеется два: 1) подвижность, которая определяется как сумма констант скоростей прямой и обратной реакции, и 2) термодинамическое сродство, которое определяет положение точки равновесия. [35]
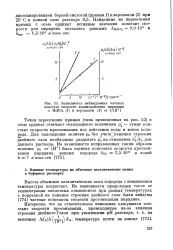 |
Зависимость наблюдаемых частных. [36] |
Точки пересечения прямых ( типа приведенных на рис. 52) е осью ординат отвечают кажущимся величинам pjj - сумме констант скорости протонизации под действием воды и ионов водорода. Для нахождения величин р0 без учета влияния строения двойного слоя необходимо разделить р0 на отношение kA / kA для данного раствора. [37]
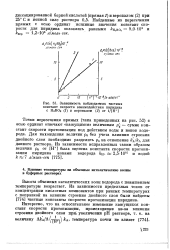 |
Зависимость наблюдаемых частных. [38] |
Точки пересечения прямых ( типа приведенных на рис. 52) с осью ординат отвечают кажущимся величинам p j - сумме констант скорости протонизации под действием воды и ионов водорода. Для нахождения величин р0 без учета влияния строения двойного слоя необходимо разделить р0 на отношение & А / & А для данного раствора. [39]
Третичные гидропероксиды распадаются преимущественно с образованием молекулярных продуктов с константой скорости km, которая в общем случае может быть суммой констант скорости гемолитического и гетеролитического распада. [40]
С - константа, определяемая условиями эксперимента, [ S0 ] - концентрация горячих молекул тетрацена и ks - : сумма констант скоростей всех каналов распада состояния S, за исключением синглетного деления; круглыми скобками, содержащими поле Н, обозначен член, чувствительный к магнитному полю. При низких температурах ( 160 К), когда деления не происходит, у ( Н) [ 5 § ] ks и интенсивность F ( H) становится не зависящей от магнитного поля. [41]
Отсюда видно, что превращение исходного вещества протекает, как и при реакции первого порядка, причем константа скорости равна сумме констант скоростей отдельных реакций. [42]
Кинетическое уравнение (21.3) для разложения вещества в параллельных реакциях имеет вид уравнения, первого порядка, в которое вместо одной константы скорости входит сумма констант скорости отдельных стадий. [43]
Таким образом, показано, что эффективная константа скорости роста в принципе может быть ( хотя и с экспериментальными трудностями) представлена как сумма констант скорости роста свободных ионов, сольватно разделенных ионных пар и контактных ионных пар. [44]
Это уравнение отличается от аналогичного уравнения ( I, 12) для реакции первого порядка тем, что в уравнении ( 1 72) стоит сумма констант скоростей обеих параллельных реакций. [45]
Страницы: 1 2 3 4