Сумма - энергия - электрон
Cтраница 1
Сумма энергий электронов, находящихся на различных орбиталях, определяет полную энергию иона. [1]
Энергия локализованной структуры равна сумме энергий электронов, локализованных на r - той рвущейся связи, плюс энергия оставшейся системы. [2]
Внутренняя энергия молекулы может быть представлена как сумма энергии электронов и энергии колебательного движения ядер. Кроме того, молекула как целое обладает энергией вращательного и поступательного движения. Колебательные и вращательные степени свободы отсутствуют у изолированных атомов. Эти свойства специфичны только для молекул. [3]
Для больших расстояний R между атомами, очевидно, можно пренебречь влиянием одного атома на движение электрона в другом атоме, поэтому для R - oo энергия электронов просто равна сумме энергий электронов в каждом из атомов водорода. [4]
В письме участникам семинара в Тюбингене ( Германия) Паули высказал гипотезу о существовании новой электрически нейтральной сильно проникающей частицы ( нейтрона) со спином 1 / г. В - распаде с каждым электроном испускается такой нейтрон, причем сумма энергий электрона и нейтрона постоянна. Оставался вопрос: как удерживается Н, в ядре. Fermi) теории р-распада [ при этом Ферми предложил называть частицу Паули уменьшительно от нейтрон - нейтрино ( итал. [5]
 |
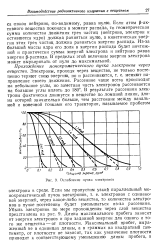
Зависимость спектра электронов / 3-распада трития от массы нейтрино ( схема. [6] |
Они являются результатами точных измерений спектра электронов от / 3-распада трития fH - 2Не е - ve вблизи его верхней границы. Сумма энергий электрона и нейтрино, равная разности энергий соответствующих уровней исходного и конечного ядер, постоянна. [7]
Наличие этих частичек и объясняет существование сплошного спектра энергий при р-радиоактивном распаде. Сумма энергий электрона ( позитрона) и антинейтрино ( нейтрино) является постоянной величиной, причем чем больше энергии несет электрон или позитрон, тем меньше энергии приходится на долю антинейтрино или нейтрино. [8]
Полная энергия может быть аппроксимирована суммой энергии электрона и межъядерного отталкивания. Последняя может быть рассчитана в рамках классической теории, и проблема сводится к расчету первого члена. [9]
Стабильность подобных гибридов, образованных из атомов, возбужденных и находящихся на высшем энергетическом уровне, может показаться аномальной. Действительно, можно различать электронную энергию молекулы или кристалла, сумму энергий электронов различных атомов их составляющих и электронную энергию этих атомов, как бы изолированных в их основном состоянии. Различие этих энергий позволяет получить энергию связи в зависимости от числа существующих связей, которая, по Полингу [11], пропорциональна наложению орбитальных функций. [10]
 |
Ослабление пучка электронов. [11] |
Если атом р-ак-тивного вещества покоился в момент распада, то геометрическая сумма количества движения трех частиц ( нейтрино, электрон и оставшееся ядро) должна равняться нулю, а кинетическая энергия этих трех частиц должна равняться энергии распада. Из-за большой массы ядра его доля в энергии распада будет ничтожной и практически сумма энергий электрона и нейтрино равна энергии р-распада. В пределах этой величины энергия электрона может вырьировать от нуля до максимальной. [12]
Мерой энергии химической связи является изменение энергии электронов при переходе от атомов к молекуле. Из энергетической диаграммы ( рис. 4.19) видно, Что это изменение энергии может быть оценено как модуль разности энергий двух электронов на связью вающей МО, 2е ( тсв), и суммы энергий электронов АО изолированных атомов, е ( 1 н) и е ( прэ) - В ряду молекул HF, HC1, НВг, HI энергия связи уменьшается. [14]
Математическая идея одного из таких методов физически соответствует следующей качественной модели. Каждый электрон в молекуле рассматривается как находящийся на определенной молекулярной орбитали ( подобно электрону в атоме, находящемуся на определенной атомной орбитали), которая охватывает всю совокупность атомов молекулы и характеризуется определенной энергией Общая энергия молекулы равна сумме энергий электронов на занятых МО. [15]
Страницы: 1 2
