Соответствующая статистическая сумма
Cтраница 1
Соответствующие статистические суммы отмечены штрихом. Верхний уровень, соответствующий отдельным атомам, принимается за нуль. [1]
Энтропия такого переходного состояния менее положительна, а соответствующая статистическая сумма мала. [3]
Произведение моментов инерции, входящее в (2.54) р можно выразить через соответствующие статистические суммы. [4]
В этом выражении удобно заменить моменты инерции внутреннего вращения fi, выразив их через соответствующие статистические суммы. [5]
А В - С) концентрация активированных комплексов, как мы видели, может быть определена при помощи соответствующих статистических сумм. Отличие Кф от обычной константы равновесия, по существу, заключается только в том, что из статистической суммы активированного комплекса исключен множитель, соответствующий движению вдоль реакционной координаты. Остальные множители, входящие в Z /, отвечают таким же степеням свободы, как в любой устойчивой молекуле. [6]
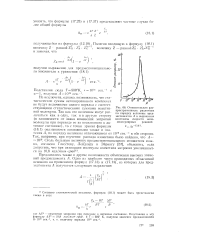 |
Относительная распространенность различных по порядку величины пред-экспонентов А в выражении константы скорости мономолекулярных реакций. [7] |
Не исключена, однако, возможность, что статистические суммы активированного комплекса не будут величинами одного порядка с соответствующими статистическими суммами неактивной молекулы. Так как эти величины могут различаться как в одну, так и в другую сторону ( в зависимости от знака изменения энтропии молекулы при переходе ее из неактивного в активное состояние), то с точки зрения формулы (18.1) оказываются возможными также и значения А, по порядку величины отличающиеся от 1013 сек. [8]
Как видно, в исходном состоянии как для метилформиата, так и для метилацетата имеется одна, дважды вырожденная конформация с е 0 ( отсутствуют отталкивания скошенных конформации, вследствие чего соответствующие статистические суммы равны 2 и в выражении ( X. В активированном состоянии для метилформиата существуют две конформации. [9]
В точке фазового перехода термодинамические функции системы должны иметь те или иные особенности: они сами или их производные должны иметь конечные или бесконечные скачки. В статистической физике все термодинамические функции выражаются через соответствующие статистические суммы или интегралы. [10]
Мы видим, что величина U0 является существенной молекулярной постоянной. Она может быть определена из термодинамических данных, если удается оцепить соответствующую статистическую сумму. [11]
Как видно, теория кинетических изотопных эффектов целиком базируется на методе переходного состояния. В теоретических расчетах изотопных эффектов неточности или недостоверности предположений о конфигурации активированных комплексов в некоторых случаях могут не играть существенной роли, если соответствующие статистические суммы сокращаются. Однако, с другой стороны, отсутствие точной информации о параметрах активированных комплексов здесь может и усилить приближенность получаемых значений. Тогда не исключено, что вообще в некоторых конкретных случаях такие расчеты станут нецелесообразными, поскольку здесь уже недостаточно совпадения с опытом только в пределах порядка величин. [12]
Это уравнение получено из конформационных схем, изображенных на рис. VI. Как видно, в исходном состоянии как для метилформиата, так и для метилацетата имеется одна дважды вырожденная конформация с OS 0 [ отсутствуют отталкивания групп в гош-положении, вследствие чего соответствующие статистические суммы равны 2 и в выражении ( VI. В активированном состоянии для метилформиата существуют две конформации. Одна из них характеризуется наличием двойной энергии UQ гош-1 4-отталкивания между метальным углеродом метоксигруппы и атомами кислорода; вторая, дважды вырожденная, связана только с одним подобным отталкиванием. В случае метилацетата первая конформация имеет такую же энергетическую характеристику, вторая же обладает добавочной энергией 1 - 4-отталкивания между углеродами ацильного и алкильного метилов. [13]
На первом этапе были вычислены термодинамические функции компонент воздуха и константы равновесия возможных реакций диссоциации и ионизации между компонентами. На этом этапе задача фактически сводилась к вычислению соответствующих статистических сумм для внутренних степеней свободы частиц. На втором этапе был вычислен состав воздуха при различных температурах и давлениях. [14]
Даже если можно построить полную энергетическую поверхность, это еще далеко не означает, что можно рассчитать абсолютную скорость химической реакции. Как было показано ранее, в реакциях принимают в общем случае участие вещества с широким спектром энергий теплового возбуждения. Поэтому необходимо применить методы статистической механики для расчета соответствующих статистических сумм веществ, принимающих участие в реакции, и активированного комплекса, рассматривая последний как обычную молекулу, за исключением вопроса о колебательной частоте вдоль координаты реакции. Таким образом, в теории переходного состояния вначале рассчитывают полную поверхность потенциальной энергии и на основании этого определяют форму активированного комплекса. Затем используют полученные длины связей, валентные углы и силовые постоянные для расчета соответствующих статистических сумм. Полагают, что реагирующие вещества находятся в равновесии с активированным комплексом, который с фиксированной скоростью распадается на продукты реакции. [15]
Страницы: 1 2
