Различное влияние - растворитель
Cтраница 1
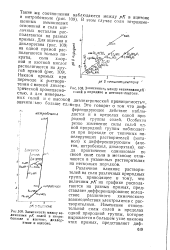 |
Зависимость между величинами.. / ( солей в пиридине и метилэтрлкетоне. [1] |
Различное влияние растворителей на соли различных природных групп, приводящее к - тому, что величины рК на графике располагаются на разных прямых, представляет дифференцирование вследствие различного химического взаимодействия электролитов с растворителями. [2]
Этим объясняется различное влияние растворителей на положение равновесия в разных кето-енольных системах. [3]
 |
Определение рК кислот в 70 % - ном растворе диоксана по рТС в воде. [4] |
Из рисунка видно также различное влияние растворителя на еноль-ную и кетонную формы кетоенолов. [5]
ПЗ-состояния, может наблюдаться различное влияние растворителей на взаимное положение этих состояний. Так, в полярных растворителях ( например, в спирте) самыми нижними могут быть 3 ( я, я) 1 и ПЗ-состояния. В результате этого в полярных растворителях наблюдается увеличение. [6]
Из рисунка видно также различное влияние растворителя на еноль-ную и кетонную формы кетоенолов. Так как анионы енольных и кетонных форм идентичны, дифференцирующее действие растворителей на их силу обязано различию в энергии взаимодействия их молекул с различными растворителями. [7]
В этой связи становится понятным различное влияние растворителя на скорость реакции при увеличении количества катализатора. В растворах - гептана гексин-1 лучше адсорбируется на поверхности катализатора вследствие отсутствия конкуренции с молекулами растворителя, которые практически не адсорбируются. Скорость реакции в этих условиях, в сильнейшей степени лимитируется активацией водорода и почти вся поверхность занята молекулами гексина. [8]
Характерной особенностью для изученного ряда ионных пар является существенно различное влияние растворителя на их реакционную способность в зависимости от природы противоиона. [9]
Указанные наблюдения имеют большое значение в аналитической химии. Различное влияние растворителя на электролиты используют для решения разнообразных аналитических задач. [10]
Для установления параметров полярности растворителя и, как следствие, степени сольватации им полярного переходного состояния были предложены различные спектроскопические методы. В этом направлении наиболее важны работы Косовера и аналогичные им работы Димрота и Райхардта по изучению сольватохро-мии - явления изменения цветности соединений при смене растворителей. Сольватохромия наблюдается вследствие различного влияния растворителей на энергии основного и возбужденного состояния. [11]
Для становления параметров полярности растворителя и, как следствие, степени сольватации им полярного переходного состояния были предложены различные спектроскопические методы. В этом направлении наиболее важны работы Косовера и аналогичные им работы Димрота и Райхардта по изучению сольвато-хромии - явления изменения цветности соединений при смене растворителей. Сольватохромия наблюдается вследствие различного влияния растворителей на энергию основного и возбужденного состояний. [12]
Страницы: 1