Металлическая сурьма
Cтраница 1
Металлическая сурьма из-за своей хрупкости применяется редко. Однако, поскольку сурьма увеличивает твердость других металлов ( олова, свинца) и не окисляется при обычных условиях, металлурги нередко вводят ее в состав различных сплавов. Число сплавов, в которые входит элемент № 51, близко к двумстам. [1]
Металлическая сурьма применяется в сплавах типографских ( до 26 %), подшипниковых ( до 18 %) и для художественных отливок. [2]
Металлическая сурьма в археологических находках встречается редко. [3]
Металлическая сурьма не изменяется на воздухе, но при нагревании окисляется в четырех-окись Sb2C4; непосредственно взаимодействует с галоидами, например с хлором, образуя SbC. С водородом сурьма образует соединение стибин SbH8 - сурьмянистый водород, являющийся весьма ядовитым; с кислородом сурьма соединяется, давая амфотерные окислы Sb2O8, Sb2C4 и кислотный окисел Sb2O6, которым соответствуют амфотерные гидраты H8SbO3, H4Sb2O5 и кислоты: метасурьмяная HSbO3, пиросурьмяная Н4 Ь2О7 - 2Н2О и орто-сурьмяная H3SbO4, и соответствующие соли. В природе сурьма встречается в самородном виде, но главным образом в виде соединений с серой: стибнит - сурьмяный блеск Sb2Ss и ряд других соединений. Сурьма применяется главным образом для приготовления сплавов: типографский сплав ( содержит 13 - 30 / Sb), британский металл ( 5 - 10 % Sb); баббиты ( содержат около 10 % Sb) и ряд других. В табл. 30 приведены свойства соединений сурьмы. [4]
Металлическая сурьма имеет белый цвет и сильный блеск, сохраняющийся на воздухе без изменения, потому что она при обыкновенной температуре не окисляется. Она кристаллизуется ромбоэдрами и имеет весьма явственно кристаллическое сложение, которое придает ей совсем иной вид, чем у большинства до сих пор знакомых нам металлов. Сурьма хрупка, так что легко превращается в порошок; уд. Накаленная на воздухе, напр. Этот окисел носит обыкновенно название окиси сурьмы, хотя его с таким же правом можно наз-вать и сурьмянистым ангидридом. Первое название придают ему потому, что в большинстве случаев употребляются соединения его с кислотами; но также легко получаются и щелочные соединения. [5]
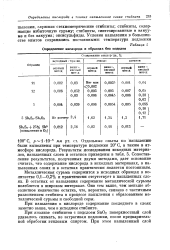 |
Определение кислорода в образцах без подслоя. [6] |
Металлическая сурьма содержится в исходных образцах в количестве 0 1 - 0 2 % и практически отсутствует в напыленных слоях. В остатках от напыления содержание металлической сурьмы колеблется в широком интервале. Оно тем выше, чем меньше абсолютное количество остатка, что, вероятно, связано с частичным разложением стибнита в процессе напыления с образованием металлической сурьмы и свободной серы. [7]
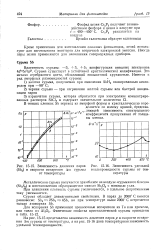 |
Зависимость давления паров.| Зависимость удельной теплопроводности сурьмы от температуры. [8] |
Металлическая сурьма получается при обжиге на воздухе сурьмяного блеска ( Sb2S3) и восстановлении образующегося окисла Sb. [9]
Металлическая сурьма была известна и применялась еще в древние времена, так как этот элемент достаточно распространен в природе и очень легко выделяется в чистом состоянии. [10]
Металлическая сурьма, полученная цементацией на цинке или железе, содержит 84 - 94 5 % чистого металла, а сурьма, полученная восстановлением окиси сурьмы, содержит 95 - 97 % чистого металла. Полученная электролитическим путем сурьма наиболее чиста. Самые распространенные примеси в металлической сурьме - это железо, мышьяк, свинец, медь, цинк и сера. [11]
Металлическая сурьма не растворяется в соляной ( в отличие от олова) и в разбавленной серной кислотах. Однако растворяется в конц. [12]
Металлическая сурьма используется как катализатор галогени-рования. Из металлической сурьмы готовят электроды, применяемые в измерении рН растворов. [13]
Металлическая сурьма практически нерастворима в холодных разбавленных минеральных кислотах, но легко растворяется в горячей серной кислоте. [14]
Металлическая сурьма выделяется в виде черного осадка на поверхности металла. [15]
Страницы: 1 2 3 4