Существование - изотоп
Cтраница 2
 |
Радиоактивный ряд урана ( числа в скобках - период полураспада в годах, днях, часах и т. д. соответственно. [16] |
Первое представление о существовании изотопов возникло при исследовании радиоактивных рядов. Альфа-распад понижает порядковый номер элемента на 2 единицы и массовое число на 4 единицы, а бета-распад повышает порядковый номер на 1 единицу и практически не влияет на массовое число. [17]
Первое представление о существовании изотопов возникло при исследовании радиоактивных рядов. Альфа-распад понижает порядковый номер элемента на 2 единицы, а массовое число на 4 единицы, тогда как бета-распад будет повышать порядковый номер на 1 единицу и практически не будет влиять на массовое число. [18]
Первые данные о существовании изотопа, более тяжелого, чем водород, были получены спектральным путем. [19]
В настоящее время установлено существование изотопов у всех химических элементов. [20]
Следует отметить, что существование изотопов задолго до работ зарубежных ученых было предсказано гениальным русским химиком А. М. Бутлеровым в 18С6 г. Тогда же Бутлеров правильно предположил и причину дробности многих атомных весов элементов. [21]
Для большинства элементов факт существования изотопов не так уж важен в повседневной практике физиков и химиков ибо разница масс изотопов относительно невелика и их свойства почти одинаковы. [22]
Сразу же после открытия существования изотопов было предложено применить этот метод для их разделения. [23]
Фундаментальное подтверждение гипотезы о существовании изотопов обязано появлению способа пространственного разделения моноэнергетических заряженных частиц в магнитном поле по отношению их массы к заряду. С 1919 по 1923 г. Астоном [3] было неопровержимо доказано существование изотопов у неона, лития, гелия, водорода, азота, криптона и других элементов. Позднее масс-спектрографическим методом были определены значения дефектов массы для дублетов на легких элементах. [24]
Первые экспериментальные данные о существовании изотопов, как разновидностей атомов данного химического элемента, различающихся по массе ядер, были получены в 1906 - 1910 гг. при изучении свойств радиоактивных элементов. Содди был предложен и сам термин изотоп. Отметим, что под термином изотоп подразумевают и ядра таких атомов. Только изотопы водорода, в отличие от всех остальных, имеют собственные названия. Под символом Н в ядерной физике часто понимают только изотоп водорода Н, получивший название протий. Отметим, что нуклиды, содержащие одинаковое число нуклонов ( протонов и нейтронов) называются изобарами, а содержащие одинаковое число нейтронов - изотопами. [25]
Как это ни странно, существование изотопов у водорода было открыто гораздо позже, чем у других элементов. Долгое время считали, что у водорода не может быть изотопов. Поэтому было предложено даже признать атомный вес водорода универсальной физической постоянной. Однако в 1932 г. американский физико-химик Юри предпринял спе -, циальное исследование, имевшее своей целью обнаружение изотопии у водорода. [26]
Протонно-нейтронная теория строения ядра объясняет существование изотопов различных элементов. Так как свойства химических элементов определяются зарядом ядер его атомов, то становится понятным, что изменение числа нейтронов в ядре изменяет только атомную массу, но не изменяет заряда ядер, а следовательно, и химических свойств этих атомов. Таким образом, различные изотопы данного элемента отличаются между собой только числом нейтронов, входящих в состав ядер атомов; число протонов же у них одинаково. [27]
Так же объясняется и возможность существования изотопов: свойства элемента определяются не массой ( весом) его атома, а зарядом ядра этих атомов. Поэтому, если ядра имеют различные массы, но одинаковые заряды, то атомы будут иметь одинаковые химические свойства. В настоящее время доказано, что почти все элементы являются смесями изотопов. [28]
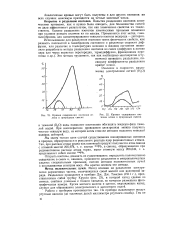 |
Кривая содержания изотопов селена в природных смесях.| Кривая содержания изотопов олова в природных смесях. [29] |
Мы знаем только один случай существования изолированных изотопов в природе, образующихся в результате распада ядер радиоактивных атомов. [30]
Страницы: 1 2 3 4