Существование - атом
Cтраница 2
Суммировать химические доказательства существования атомов и химические методы, позволяющие определить их массы. [16]
После того как возможность существования атомов и радикалов была надежно установлена и целесообразность их исследования достаточно обоснована, начались работы по созданию количественных методов идентификации структуры радикалов, участвующих в тех или иных процессах, и измерения их в реальных химических системах. [17]
Однако все же следует допустить существование атомов кислорода между атомами А1 и Р, так как 2 / 3 тетраэдров содержат один из этих атомов. В элементарную ячейку цеолита P-L входят 4 е-ячейки, каждая из которых содержит примерно 6 Si. [18]
Второй же критерий устанавливает прекращение существования атома и, соответсвенно, полное отсутствие спектральных линий. [19]
Задолго до этого гипотеза о существовании атомов неоднократно доказывала свою плодотворность при объяснении самых различных физических и химических явлений. Тем не менее ее становление было сопряжено с громадными трудностями как научного, так и мировоззренческого порядка. [20]
Более того, в решетке возможно существование атомов одного и того же элемента, например, Fe, с различным зарядом. Требование целочислен-ности отношений атомных концентраций уже не вытекает из соотношения зарядов ионов-партнеров и тем самым не играет в такой мере регулирующей роли. Многочисленные виды микродефектов 1-го рода становятся возможными, а с ними - различные дробные соотношения коэффициентов х и у, характеризующих основной состав вещества. [21]
В конце XIX века было выяснено существование атомов электричества - элементарных заряженных частиц. Целый ряд открытий привел ученых к мысли о том, что атомы химических элементов должны состоять из этих элементарных частиц. [22]
Этот последний промежуток т соответствует времени существования атома в возбужденном метастабильном состоянии. Величину т принято называть продолжительностью жизни метастабильного атома. [23]
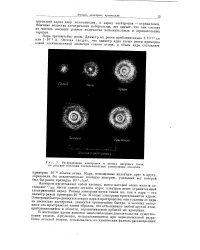 |
Распределение электронов в атомах инертных газов. на рисунке показаны последовательные электронные оболочки. [24] |
В настоящее время имеются многочисленные доказательства существования атомов. [25]
Сегодня, конечно, никто в существовании атомов и субатомных частиц не сомневается. При этом ощущение абстрактности микромира исчезло не полностью. Оно питается истинной непохожестью законов микромира на привычные законы макромира. [26]
Эти ученые исходили из убеждения в реальности существования атомов ( молекул) и основывали свои выводы: первые двое - на законах механики, последний - на теории вероятности. [27]
По мнению Роско и Гардена, теория существования атомов различного веса привела Дальтона к открытию фактов соединения в кратных отношениях [ 2, стр. Действительно, если атомы неделимы и, по предположению Дальтона, соединяются друг с другом не только в отношении 1: 1, но и в других, обычно довольно несложных численных соотношениях, очевидно, что и состав различных веществ в тех случаях, когда два элемента дают несколько соединений, должен подчиниться закону кратности весовых отношений. В течение августа и сентября 1804 г. Дальтон исследовал составы метана и этилена, правильно установив соотношение количества водорода и углерода в этих соединениях. [28]
Как известно, необходимость объяснения свойств и самого существования атомов послужила в свое время толчком к развитию квантовой физики. Уже изучение простейшего атома водорода показывает, что устойчивость и размеры отдельного атома обусловлены принципом неопределенности, препятствующим тому, чтобы электрон с определенной энергией находился слишком близко к ядру атома. [29]
Однако с точки зрения классической физики нельзя было объяснить существование стабильных атомов такой структуры, так как в соответствии с законами электродинамики всякий электрон, движущийся по окружности вокруг ядра, должен терять свою энергию на излучение, постепенно приближаться к ядру и в конце концов упасть на него. При этом должна непрерывно меняться частота обращения электрона вокруг ядра и, следовательно, частота испускаемого атомом излучения. В то же время было известно, что атомные спектры имеют строго определенный дискретный и стационарный характер. [30]
Страницы: 1 2 3 4