Существование - равновесие
Cтраница 3
В этой модели предполагается существование равновесия между локализованными и делокализованны-ми, квазисвободными электронами. Таким образом, как уже говорилось в разд. [31]
Во втором возможном случае существования равновесия газ - газ критическая кривая, отходящая от критической точки Кг наименее летучего компонента, направляется в сторону более низких температур, проходит в точке D через температурный минимум и поворачивает в сторону более высоких температур. [32]
Это уравнение выражает условие существования равновесия между кристаллитом и дефектным граничным слоем. При постоянном г, каждой температуре отвечает определенная длина Правп, для которой выполняется условие равновесия. В следующем разделе рассматриваются значения таких равновесных длин при использовании различных моделей. [33]
В связи с фактом существования равновесия воды, любой водный раствор приходится рассматривать как некую сложную равновесную систему. [34]
Ц-4, или о существовании равновесия между близкими по энергии синглетным и триплетннм состояниями, в котором синглетное состояние преобладает. [35]
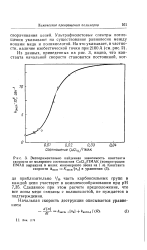
Ультрафиолетовые спектры поглощения указывают на существование равновесия между ионами меди и поликислотой. [37]
По-видимому, это указывает на существование равновесия между сольва-тированными и несольватированными молекулами, которое зависит от природы растворителя, аналогично тому, что наблюдается в УФ-спектре. [38]
В разделе 4.3 исследуется вопрос существования равновесий в системе. [39]
Это приводит к выводу о существовании равновесия между активными и неактивными молекулами, причем предполагается, что действие катализатора сводится к сдвигу равновесия в сторону образования активных молекул. Такой вывод нельзя, однако, признать правильным, так как увеличение числа активных молекул должно было бы сдвинуть равновесие самой катализуемой реакции, чего мы никогда не наблюдаем. Принимая теорию Аррениуса, мы можем из нее вывести только то, что катализатор ускоряет достижение равновесия между неактивными и активными молекулами. Но это не говорит ничего, кроме того, что мы уже знаем: что катализатор влияет на скорость реакции. Эта теория ( в ее первоначальной форме) не дает нам объяснения каталитического действия и потому не может служить удовлетворительной рабочей гипотезой. [40]
При таких давлениях есть основание предполагать существование равновесия по крайней мере в зоне максимальной температуры, так как процессы ионизации и диссоциации, в которых участвуют две микрочастицы, должны протекать быстрее процесса рекомбинации, в котором участвует три частицы. Они показали, что на высоте 30000 м ( p - 10 - 2 ат) при Моо 20 на расстоянии 1 м от передней кромки 80 % кислорода находится в равновесии. Экстраполяция этих результатов на процесс ионизации NO неправомерна, так как скорости реакции в этом случае другие. Но поскольку для протекания реакции необходим атомарный кислород, то можно предполагать, что при высоких числах Маха атомарного кислорода будет достаточно для протекания этой реакции. [41]
Важнейшая особенность процессов сорбции - это существование равновесия между фазами в сорбционной системе, которое определяется только физико-химическими свойствами системы и является ее термодинамической характеристикой. [42]
В последнее время работой [72] установлено существование равновесия N2O4 NO NO и поэтому не исключено, что комплекс с олефином облегчает возникновение в первичном акте нитрозилнитратов. Гетероли-тическому механизму способствует увеличение полярности растворителя. Повышение температуры и разбавление неполярным растворителем облегчает реакцию, идущую по гемолитическому механизму. [43]
Месробиан и Тобольский 154а ] доказали существование равновесия полимеризация-деполимеризация. Они выдерживали различные толуольные растворы смесей стирола и полистирола одной и той же весовой концентрации при 100 при освещении кварцевой лампой на воздухе и нашли, что вязкости всех этих растворов постепенно приближаются к одному и тому же значению. Если эта тенденция к достижению одного и того же среднего молекулярного веса системы связана с достижением действительного термодинамического равновесия, то оно должно быть результатом некоторых или даже всех реакций агрегации и дезагрегации, протекающих при полимеризации и деполимеризации. Принимается, что радикал R образуется в результате некоторого процесса инициирования. [44]
Изменение знака эффекта Коттона навсегда означает существование конфор-мационного равновесия. [45]
Страницы: 1 2 3 4