Существование - критическая точка
Cтраница 1
Существование критической точки обусловлено действием межмолекулярных сил. Вследствие этого параметры критической точки представляют собой важнейшие характеристики вещества, которые в обобщенной количественной форме выражают эффект действия межмолекулярных сил. [1]
Существование критической точки на кривой равновесия жидкости и пара отчетливо демонстрирует отсутствие принципиальной разницы между жидким и газообразным состояниями вещества. Поясним это следующим примером. [2]
Существование критической точки делает возможным непрерывный переход между любыми состояниями газа и жидкости по пути, не пересекающему кривую равновесия фаз и, следовательно, ни в какой момент не приводящему к расслоению фаз. Вдоль такого пути возможно и аналитическое продолжение термодинамических величин из области газообразного состояния в область жидкого состояния. Тем самым становится условным само понятие о различии газообразной и жидкой фаз. Строго о двух таких фазах можно говорить лишь тогда, когда они обе сосуществуют одновременно. Последнее позволяет понять отсутствие критической точки на кривой сосуществования твердого кристаллического тела с любой другой фазой. Благодаря присущему элементу симметрии, кристаллическое состояние качественно отличается от любого другого однородного состояния и потому всегда может быть однозначно опознано. [3]
Существование критической точки показывает, что между жидким и газообразным состоянием нет принципиального различия. Переход па прямой АВ между теми же начальным и конечным состояниями идет со скачкообразным изменением свойств вещества. [4]
Существование критической точки обусловлено наличием молекулярных сил. Вследствие этого параметры критической точки представляют собой, как уже отмечалось ранее, важнейшие характеристики вещества, которые в обобщенной количественной форме выражают эффект действия межмолекулярных сил. Так, например, критическая температура самым прямым образом связана с величиной потенциальной энергии взаимодействия молекул. [5]
Существование критической точки, как это было показано в § 4 - 3, впервые доказал Д. И. Менделеев в 1860 г. Значение температуры в критической точке он назвал абсолютной точкой кипения данной жидкости. [6]
Существование критической точки не противоречит специфическому поведению раствора в ее окрестности. В частности, вблизи критической точки раствора, так же как и в окрестности критической точки чистого вещества, легко реализуются неустойчивые состояния. [7]
Существование критической точки высшего порядка в системе этан - пропан - метанол не вызывает сомнений. Эта точка, по нашим данным, должна реализоваться при температуре около 74 С и давлении около 57 атм. [8]
Поэтому существование критической точки возможно только у таких фаз, между которыми допустим непрерывный переход. Такими фазами, по-видимому, могут быть лишь газ и жидкость, так как они отличаются друг от друга большей или меньшей степенью взаимодействия между молекулами. [9]
Поэтому существование критической точки возможно только у таких фаз, между которыми допустим непрерывный переход. Такими фазами, по-видимому, могут быть лишь газ и жидкость, так как они отличаются друг от друга большей или меньшей степенью взаимодействия между молекулами. [10]
Факт существования критической точки доказывает сделанное выше утверждение об отсутствии принципиального различия между газом и жидкостью. Мы видим, что возможен непрерывный переход из жидкого состояния в газообразное ( в обход критической точки) без какого бы то ни было фазового превращения. [11]
Факт существования критической точки доказывает сделанное выше утверждение об отсутствии принципиального различия ме. Мы видим, что возможен непрерывный переход из жидкого состояния в газообразное ( в обход критической точки) без какого бы то ни было фазового превращения. [12]
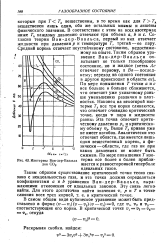 |
Изотермы Ван-дер - Ваальса для СО2. [13] |
Таким образом существование критической точки тесно связано с неидеальностью газа, и эта точка должна определяться коэфициентами а и Ь уравнения Ван-дер - Ваальса, выражающими отклонения от идеальных законов. [14]
Таким образом, существование критической точки тесно свя зано с отступлением газов or идеального состояния, и эта точк. [15]
Страницы: 1 2 3 4