Существование - азеотроп
Cтраница 2
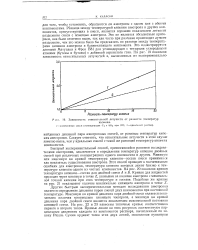 |
Зависимость относительной летучести от разности температур. [16] |
Быстрый экспериментальный способ, применявшийся ранними исследователями азеотропии, заключается в определении температур кипения двойных смесей при различных концентрациях одного компонента в другом. Минимум или максимум на кривой температура кипения-состав смеси принимался как показатель существования азеотропа. Этот способ приводит к значительным ошибкам для азеотропов, температура кипения которых лежит близко к температуре кипения одного из чистых компонентов. На рис. 20 показана кривая температура кипения-состав для двойной смеси А и В. Кривая для жидкостей проходит через минимум в точке Z, указывая на наличие азеотропа с минимальной точкой кипения при этих температуре и составе. [17]
Проведенное нами экспериментальное исследование бинарных и тройных подсистем показало, что в системе существуют максимальный аэеотроп м-крезол - п-метилацетофенон и положительный азеотроп крезол - изопропенилтолуол; остальные подсистемы гексатопа зеотропны. Ни в одной из рассмотренных тройных подсистем не обнаружены тройные азеотропы и, следовательно, исключена возможность существования азеотропов высшей размерности. [18]
Трудность разделения этих веществ объясняется сближением температур кипения нафталина и смеси фенолов в условиях, существующих в верхней части фракционной колонны. Таким образом, путем эффективной ректификации можно разделить фенолы и нафталин, чем ставятся под сомнение утверждения отдельных исследователей о существовании азеотропов фенолов и нафталина. [19]
Ректификация этой смеси производилась при различных давлениях в интервале от 760 до 8 мм рт. ст., что соответствует интервалу температур кипения уксусной кислоты от 118 3 до 16 6 С. В исследованном интервале давлений и температур существования азеотропа не обнаружено. [20]
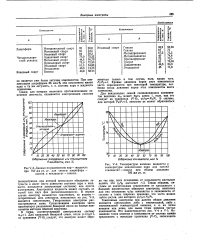 |
Температуры кипения жидкости и. [21] |
В первом случае азеотроп называется гомогенным, во втором - гетерогенным. Два азеотропа, показанные на рис. V-3, являются гомогенными. Гетерогенные азеотропы рассматриваются ниже. Существование азеотропа часто препятствует разделению бинарной смеси на чистые компоненты методом обЫчной перегонки. [22]
Однако отличительные черты систем с азеотропизмом не сводятся только к специфическому поведению самой азеотропной смеси. Они проявляются и за ее пределами. Особенно отчетливо это заметно в характере объемного поведения подобных систем. Действительно, например, существование азеотропа уже при низких давлениях приводит к появлению экстремума на линии газа изотермы равновесия v - Ni, причем состав в точке этого экстремума не совпадает с составом азеотропа. В гомогенной области газообразной ( для положительного азеотропа) фазы изобары - изотермы v - Ni должны обязательно проходить через максимум, что влечет за собой, как будет показано далее, появление особенностей в концентрационной зависимости ряда термодинамических величин. Появляются, как мы увидим, и другие очень важные следствия. [23]
Установлено [42] общее правило, определяющее влияние давления на состав азеотропных смесей. С повышением температуры кипения азеотропа с минимумом на кривой кипения состав этой смеси изменяется в сторону увеличения содержания компонента, обладающего большей скрытой молекулярной теплотой испарения. В случае азеотропных смесей с максимумом на кривой кипения при повышении температуры кипения, наоборот, увеличивается концентрация компонента с меньшей скрытой молекулярной теплотой испарения. Однако имеются многочисленные исключения из этого правила, так как некоторые системы обнаруживают существование азеотропа с максимумом на кривой кипения только при определенном давлении. [24]
Особого внимания заслуживает другой двуположительно-отри-цательный азеотроп [ ( - ) А, Р () Т ], где А - уксусная кислота, Р - пиридин и Т - толуол. Первые опыты с указанным азеотро-пом проведены Змысловской, но результаты не публиковались, так как не было убежденности в достаточной чистоте толуола. Все примеси, обнаруженные в толуоле, уменьшали показатель преломления. При ректификации толуола наблюдается то же явление, которое было описано Андерсоном для нитрационного бензола: все примеси отгонялись при более высокой температуре бензола, так как они образуют тангенциальные или почти тангенциальные изобары температур кипения. Противоречие между двумя опытами Лека ( 1918 г.), в первом из которых существование азеотропа пиридин - толуол отрицалось, а во втором - подтверждалось, было разрешено в пользу последнего. Состав и температура кипения положительного бинарного азеотропа ( Р, Т), определенные эбуллиометрическим методом, оказались равны: 20 05 вес. [25]
Страницы: 1 2