Существование - гидрат
Cтраница 2
Область существования гидратов на этом графике располагается левее и выше приведенных кривых. Из рис. 2 видно, что с повышением давления и плотности газа возрастает температура образования гидрата. Так, для газа с р 0 6 при давлении 25 кгс / см2 гидраты образуются при температуре 7 4 С, а для газа с р 0 7 - при температуре 10 1 С. С увеличением давления возрастание температуры гидратообразования в зависимости от плотности газа становится менее значительным. Например, при давлении 150 кгс / см2 газ с р 0 6 образует гидраты при температуре 20 5 С, а газ с р 0 7 -при температуре 21 6 С. [16]
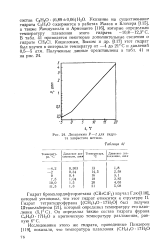 |
Диаграмма Р - t для гидрата хлористого метила. [17] |
Указание на существование гидрата С2Н4О содержится в работах Мааса и Бломера [115], а также Маццукелли и Арменанте [116], которые определили температуру плавления этого гидрата - 10 8 - 12 3 С. Кошелевым, Быком и др. [117] этот гидрат был изучен в интервале температур от - 4 до 21 С и давлений 0 5 - 5 атм. [18]
Установлено также существование гидратов аргона, криптона, ксенона и радона, получающихся при сжимании газа над водой до давлений, превышающих упругость диссоциации. Для гчдрата аргона это давление при 0 равно 98 ат, а для гидратов криптона и ксенона соответственно 14 5 и 1 15 ат. Гидрат неона при этих условиях не был получен, даже под давлением до 250 ат. [19]
Для доказательства существования гидрата радона и для изучения некоторых его свойств можно применить один из новейших методов физико-химического анализа. В связи с тем, что получение твердого гидрата радона невозможно, необходимо провести опыт, доказывающий изоморфизм гидрата радона с гидратом обыкновенного газа известного состава. [20]
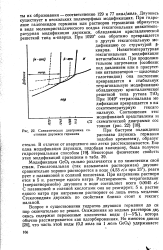 |
Схематическая диаграмма стояния двуокиси германия. [21] |
Вопрос о существовании гидратов двуокиси германия до ей пор окончательно не решен. Осажденная из водных растворов дв окись содержит переменные количества воды ( 1 - 5 %), котора обычно рассматривается как адсорбированная. [22]
Здесь также зона существования гидратов расположена левее, а зона их отсутствия - правее. Из графика видно, что для более тяжелого газа требуется значительно меньшее давление для образования гидратов при той же температуре. [23]
Из общей химии известно существование гидратов, представляющих собой соединения частиц растворенного вещества с молекулами растворителя - воды. [24]
На этих графиках область существования гидратов расположена выше t слева от кривых. [25]
Кривые рис. 4 показывают условия существования гидратов низших парафиновых углеводородов. Здесь линии AD-кривые упругости паров индивидуальных углеводородов; линии ВС - границы существования гидратов: левее линий ВС находится зона существования гидратов, правее-зона отсутствия гидратов. Точка С представляет как бы критическую температуру, выше которой при любом высоком давлении гидрат не может существовать. Кривые рис. 4 показывают, что для образования гидратов более тяжелых углеводородов требуется значительно меньшее давление при той же температуре. [26]
Существование гидрата тетраметиламмония косвенным образом подтверждает существование гидрата аммония: один достаточно устойчив и существует в самостоятельном виде, другой неустойчив и потому не может быть изолирован. [27]
На основании данных своего метода авторы предположили существование гидратов спиртов, кетонов и других разнообразных соединений. Связь должна также сказываться на поверхностном натяжении на границе раздела между двумя жидкими фазами, поскольку ассоциация влияет на равновесие, которое имеет место на границе раздела. Жирифалко и Гуд [772] ввели функцию Ф, связывающую свободную энергию адгезии между фазами со средним геометрическим свободных энергий когезии. [28]
 |
Кинетические параметры электровосстановленияNi2 и Со2 из водно-формамидных растворов. [29] |
Повышенной способностью к комплексообразованию, приводящей к существованию прочных гидратов никеля и кобальта в водных растворах, объясняется и то, что прибавление неводного растворителя ( менее активного лиганда, чем ОН -) к водным растворам этих металлов часто увеличивает обратимость их восстановления и константу скорости электродной реакции [766, 765], хотя в целом при переходе от водных растворов к неводным растворам наблюдается обратная закономерность. [30]
Страницы: 1 2 3 4 5