Равновесное существование
Cтраница 1
Равновесное существование более чем трех фаз; веществ невозможно. [1]
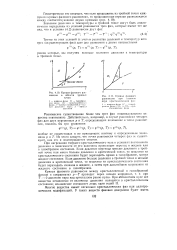 |
Кривые фазового равновесия в области тройной точки.| Кривые фазового равновесия при наличии двух кристаллических фаи. [2] |
Равновесное существование более чем трех фаз индивидуального вещества невозможно. [3]
Область равновесного существования фазы зависит от температуры, собственного ( теплового) разупорядочения стехиомет-рического кристалла и энергии взаимодействия дефектов. [4]
Область равновесного существования модификации Y на диаграммах этого типа резко сокращена. [5]
Для равновесного существования соприкасающихся фаз прежде всего необходимо соблюдать условия механического и теплового равновесия. [6]
Распределение областей равновесного существования определенных сочетаний фаз ясно из рис. 16, а. Так, например, сплав, содержащий 20 % Bi и 80 % Cd при 225 ( точка г), представляет собой гетерогенную систему 2, состоящую из кристаллической и жидкой фаз. Чтобы определить состав этих фаз, надо провести горизонталь ( ноду) через г до пересечения с границами области, в которой лежит эта точка. [7]
ADC, ограничивающими область равновесного существования двух фаз, определяют состав фаз, на которые три данных р и t происходит распадение раствора. [8]
Особенностью систем металл-диссоциирующая примесь является равновесное существование растворенной в металле примеси и свободного газа над поверхностью расплавленного металла. Состояние равновесия определяется температурой, составом раствора, количеством металла и объемом газовой фазы. При изменении одного из параметров, характеризующих систему, происходит количественное перераспределение между раствором примеси в металле и газовой фазой. Переход от одного равновесного состояния к другому может сопровождаться выделением газовой фазы непосредственно в объеме расплавленного металла. [9]
На диаграмме состояния указаны области равновесного существования сплавов в однофазном и двухфазном состояниях. Выше линии ABCD равновесным является однофазное жидкое состояние. [10]
На рис. 1 - 1 представлены условия равновесного существования трех фаз в случае химически индивидуального вещества. Кривая сублимации ОА соответствует зависимости давления насыщенного пара над твердой фазой от температуры. [11]
 |
Гр-днпграмма. - вещество с одной гройпоЛ точкой. б - пола. в - гелий. [12] |
На этой диаграмме в тройной точке О ( равновесное существование трех фаз) пересекаются три линии, соответствующие изменению состояния равновесных двухфазных систем. На линии р - - р ( Т) ( кривой испарения) находятся в равновесии жидкая и паровая фазы. Линия р - / а ( Т) соответствует равновесному существованию твердой и паровой фаз, и ее называют кривой сублимпции. И наконец, на линии, р - р3 ( Т) равновесно существуют твердая и жидкая фазы, и она называется кривой плавления. Эти кривые разграничивают плоскости диаграммы на области, соответствующие паровой, жидкой и твердой фазам. [13]
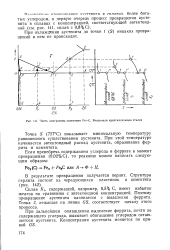 |
Часть диаграммы состояния Fe-С. Вторичная кристаллизация сталей. [14] |
Точка 5 ( 727 С) показывает минимальную температуру равновесного существования аустенита. При этой температуре начинается эвтектоидный распад аустенита, образование феррита и цементита. [15]
Страницы: 1 2 3 4